本栏目由医隆网专家团队审核!
免疫浊度测定是基于经典免疫学反应——沉淀试验的一种技术。当可溶性抗原与相应抗体在适宜条件下发生特异性结合时形成复合物 (颗粒)出现沉淀。免疫复合物的数量可以用免疫浊度技术进行检测。
1901年Emil von Behring博士由于在运用抗毒素血清预防与治疗白喉与破伤风等病症方面的功绩被授予首届诺贝尔生理学/医学奖。其后,Emil von Behring博士创建了蛋白研究和生产基地——Behringwerke成为历史上专门致力于血浆蛋白研究的第一家公司。
1959年,Sehultze和Schwick提出用抗原-抗体结合后形成复合物使溶液浊度改变,用普通比浊计测定免疫球蛋白的含量,称为透射比浊法,但是由于敏感性太差而未引起注意。
1965年,在免疫沉淀和免疫扩散的基础上,利用平板技术测定40多种血清蛋白受到科学家的关注,被认为是一种革新。但同样较为烦琐,灵敏度差,不能满足临床快速诊断的需求。
1967年,Ritchie提出用终点激光散射比浊法定量测定悬浮的免疫复合物颗粒与入射光束成一定角度时光散射的强度来评估物质含量,之后在终点散射比浊法的基础上进行改进推出了定时散射比浊法。这使经典的凝胶内沉淀法的测定由数十小时缩短至数小时,开创了蛋白免疫分析的新篇章。随之Technicon和Behring公司基于此种原理制造了自动免疫蛋白分析系统,并将计算机系统运用于该系统中。
1977年,Sternberg提出了更快速的、在抗原抗体反应最高峰时测定复合物含量的方法,称为速率散射比浊法(ratenephlometry)。由此可使抗原结合反应在几十秒之内得出检测结果,即在尚未出现肉眼可见的反应阶段就能够进行快速检测,使免疫化学分析发生了质的飞跃。
近年来,在免疫比浊法的基础上又出现了乳胶增强比浊法。该方法是利用微小的乳胶颗粒(直径1μm±)连接抗体后,在液相中与相应抗原结合后产生光吸收或光散射的变化量来测定待测抗原含量,提高了免疫比浊法的灵敏度,同时也大大减少了非特异性反应的影响,精确度和重复性都有较大提升。目前此项技术在散射比浊与透射比浊中均有较好的运用。
在乳胶增强技术的基础上,新的Durel(dual radius latex-enhanced technology)乳胶增强技术兼顾了更高的分析灵敏度及检测范围。该技术在试剂中加入两种直径大小不同的乳胶颗粒,并且对乳胶颗粒包被不同特点的抗体。在反应初期,抗原低浓度时,较大的乳胶微粒子包被有高反应性的抗体,大颗粒结合迅速,从而即使在非常低的浓度时就可产生强信号,这种作用提高了分析灵敏度;在高浓度抗原反应进入后半期时,灵敏度较小的乳胶微粒子包被有低反应性的抗体,这种作用提供了更高的检测上限,得到更好的测试表现。
短短几十年,以各种技术为原理的免疫比浊分析仪竞相问世,得益于自动化技术的发展,溯源性物质的研究,检测系统的标准化和对检验结果统一性的追求。透射比浊与散射比浊均对国际参考物质ERM-DA470(CRM470)做出了许多贡献。越来越多的实验室采用免疫比浊法进行特定蛋白检测,该法准确、经济、高效、安全,并且符合临床快速诊断的需求。
里程碑事件:
• 1955年德灵(Dade Behring)公司发现了15种人类特定蛋白。
• 1966年德灵公司免疫琼脂扩散板——Partigen面世。
• 1977年德灵公司激光散射比浊仪——BLN面世。
• 1980年全自动ICS特定蛋白分析仪上市。
• 1985年德灵公司BNA面世。
• 1986年Beckman Coulter Array®特定蛋白分析仪在中国上市。
• 1988年Dade Behring公司第一代全自动特定蛋白散射比浊仪——BN 100面世。
• 1991年Beckman Coulter Array® 360在中国上市。
• 1994年Dade Behring公司全自动特定蛋白散射比浊仪——BN Ⅱ面世。
• 1997年Beckman Coulter IMMAGE®在中国上市。
• 21世纪乳胶增强及罗氏Durel乳胶增强技术的发展。
• 2003年西门子诊断(原Dade Behring)推出Protis结果解释软件。
• 2004年Beckman Coulter IMMAGE® 800在中国上市。
• 2011年游离轻链检测项目进入中国 。
•深圳国赛生物的2011年推出的Omlipo全自动特定蛋白分析仪是国内最早的全自动特定蛋白仪器。
从1897年 Kraus描述了免疫浊度试验起至今,液相免疫浊度测定技术已经经历了透射比浊法→散射比浊法→速率散射比浊法→激光散射比浊法→免疫胶乳比浊法和速率抑制免疫比浊法。随着计算机技术的高速发展产生了基于免疫浊度测定的自动化分析仪器,目前临床实验室所应用的免疫比浊仪(特种蛋白免疫分析仪)所采用的检测技术主要有二类:一类是透射比浊法,另一类是散射比浊法。仪器也分为透射比浊仪和散射比浊仪,其区别在于光路和光接收器的路径不同,具体分类如下:
(一)透射比浊特种蛋白免疫分析仪
该仪器采用透射比浊免疫浊度技术(turbidimetry assay),最常用于生化指标的测定,用于免疫沉淀反应有一些缺陷:
1.溶液中存在的抗原抗体复合物分子应足够大,分子太小则阻挡不了光线的通过。
2.溶液中的抗原抗体复合物的数量要足够多。如果数量太小,溶液浊度变化太小,对光通量影响不大。
3.透光比浊采用光电池直接接收光通量,即光度计的灵敏度不高,微小的浊度变化不易影响透光率的改变。
4.透光比浊是依据透射光减弱的原理来定量的,因此只能测定抗原抗体反应的第二阶段,检测仍需抗原抗体温育反应时间,检测时间较长。因此,透射比浊类的自动分析仪用于免疫测定已趋减少,该测定原理也主要用于生化分析仪。
(二)散射比浊特种蛋白免疫分析仪
散射比浊分析(nephelometry assay)是一种微量、快速、自动化检测体液中特定蛋白质成分的免疫化学分析技术,该技术是将免疫测定与散射比浊法的原理相结合而设计的一种快速免疫测定方法。主要用于对体液中单个蛋白成分的测定。这类仪器主要分为:定时散射比浊仪和速率散射仪。
1.定时散射特种蛋白比浊分析仪 该反应检测系统不完全具备真正的抗原过量检测的能力,设计者仍采用抗体过量的原理来保证抗原抗体反应形成不可溶性小分子额粒,获得的小分子颗粒产生最强的散射光信号。在第一阶段即预反应时间内,检测总量的10%的标本与过量抗体反应,若第一次读数未超过预先设置的抗体浓度阈值,提示该待测样品符合预置范围,检测中不会出现抗原过量,因而把余下的90%的样品加入开始第二阶段反应;如果预反应阶段读数超过所定的阈值上限,提示待测样品的浓度含量较高,样品必须在更高稀释度下重新测定。
尽管固定时间散射比浊法也是目前应用中一种较为先进的方法,但该反应可能仍存在一些检测准确性的问题:
(1)预反应阶段与抗体反应的仅是少量抗原,因此预反应阶段的信号变动仅占全反应阶段的信号变动的极少部分,此信号值的扣减对最终的结果计算影响不大。
(2)该方法采用的是间接抗原过量检测,在反应末端并没有进行真正的抗原过量检测。代表仪器为BNⅡ全自动特种蛋白分析系统。
2.速率散射特种蛋白免疫分析仪 速率散射测定法是一种抗原抗体结合反应的动态测定法。它是免疫分析测定的一项革命,使免疫化学分析发生了质的飞跃。该法的逐步完善,使体液特定蛋白的测定更加准确和快速,成为当今临床免疫学诊断技术中的重要应用技术之一。速率散射特定蛋白免疫分析仪测定单位时间内抗原抗体反应形成复合物的最快时段的复合物颗粒的量,仪器自动通过标准曲线将速率峰值转换为所测抗原的终浓度。代表仪器为 IMMAGE全自动特种蛋白分析仪。
目前BNⅡ和BN- prospec全自动特种蛋白分析仪所用的终点法,主要用来检测乳胶增强反应的特种蛋白浓度,是检测预温30分钟后的光散射强度,通过与储存在计算机内的标准曲线进行比较即可得出该物质的浓度。免疫乳胶浊度测定带载体的免疫比浊法,其敏感性远远高于比浊法操作简单。它是选择一种大小适中、均匀一致的乳胶颗粒,吸附抗体(lgC)后当遇到相应的抗原时,则发生凝剂。单个乳胶颗粒在入射光波长之内,光线可透过。当两个乳胶颗粒凝集时,则透光度降低,降低程度与乳胶聚集成正比故与抗原量也成正比。利用此方法可进行ASO、CRP、RF和CIC等的检测。
BNⅡ和 bn-prospec特定蛋白免疫分析仪为了克服定时散射检测方法上的不足,为保障结果的准确性,仪器在检测时,采用抗原过量检测,自动化的反应前预检测、定时动态速率散射比浊和对于小分子蛋白应用了乳胶增强抗体(技术),以最优化的抗原抗体反应条件,极大地提高了分析灵敏度和精度。
检验项目参见表16-2。
表16-2 免疫比浊分析仪的应用范围
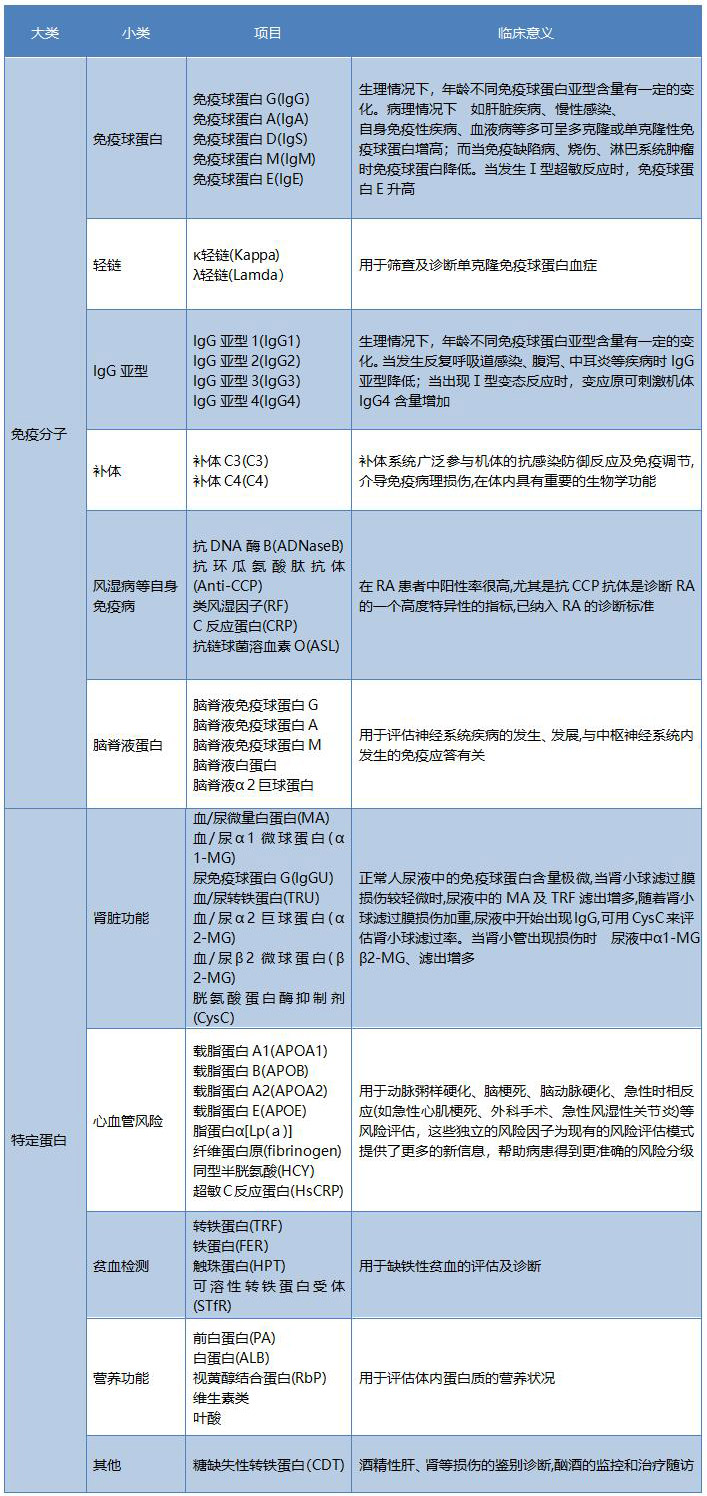
免疫比浊分析仪的使用提高了检测质量,大幅度地防止漏检、误诊的发生。为保证自动免疫比浊仪在工作中发挥更好的效果,全面执行质量控制(简称质控)工作是必不可少的,质量控制(质控)又称质量管理,系指实验室为达到质量要求,自行或由权威部门建立观察分析步骤的变异性,随时评估检测结果准确性的一系列相关制度。只有建立完善的质量管理才能及时发现检测分析过程中的误差及产生误差的原因,控制与分析有关的各个环节,防止出现不可靠的结果,以保证实验室检测结果准确性的稳定,这是达到质量保证的必要手段。
一、 免疫比浊分析仪操作人员的培训与管理
全自动免疫比浊分析仪的广泛应用对实验室工作人员提出了更大的挑战。实验室技术人员应积极、努力地去面对和适应它。同时更新自己的知识,除了学习自己本专业知识外,还应在计算机、电子学、仪器学、英语等方面提高能力,从而达到自如控制大型设备的目的。改善和加强实验室的质量控制系统,使检测结果更加准确。
二、 免疫比浊分析仪全程质量管理
(一) 仪器运行前质控
(1) 仪器的运行环境:良好的仪器运行环境是仪器安全性的必然保障。
(2) 样本类型:建议使用血清样本。血浆样本(EDTA、肝素锂和肝素钠)也可以使用。血清或血浆样本的收集应使用临床实验室常规方式。
(3) 样本采集与储存:最好使用禁食8h以上待检测者的新鲜血清或血浆。抽取标本后及时、安全地运送至实验室进行测定,采血管应一直保持垂直且密闭保存。建议在采血2h内使用物理方法将血清和细胞成分分离开来。
(4) 样本处理:如果血清样本在8h内不能进行检测,样本应保存在2~8℃。如不能在72h内进行检测,样本应在-15~-20℃冰冻保存。冰冻样本只能融化一次。如果重复冻融,样本中的分析物会发生变化。
(5) 样本量:按照不同样本管要求的最小样本量抽取。
(6) 试剂准备:试剂使用前轻柔地倒转试剂盒以混匀试剂。换上防蒸发盖并放置到仪器上。检查是否有气泡。试剂是否可以接受用于检测由质控结果决定。
(7) 试剂储存和稳定性:不合适的储存条件可能会引起错误的结果。在每天的工作完成后,将所有的试剂盒都放回冰箱中(2~8℃)。
(二) 仪器运行中的质控
实施质控需要一套完整的标准操作规程文件(SOP)作保障。如样本的采集、储存操作规程,仪器操作和维护操作规程,试剂的使用和保存规程等。
1.正确的操作程序 每台仪器都有实际操作指南,认真制作SOP文件,严格按照SOP文件正确操作以得到正确的检测结果。
2.校准品及质控品标准化 特定蛋白检测的标准品是根据临床化学国际联盟IFCC设定,并由欧共体参考品局BCR进行鉴定的血浆蛋白的国际参考品CRM470,该参考品被美国病理学家协会CAP指定为人血清蛋白(RPPHS)批号91/0619的参考品预备。
第一代参考品(即1967年推出的批号67/86的WHO免疫球蛋白标准品)用于免疫扩散和火箭电泳测定的标准化,但由于其有些浑浊不太适用于免疫比浊法。新一代国际人血清蛋白参考品RPPHS,研制RPPHS的目的是将其用来校准用于血清蛋白常规测定的第三级参考品。RPPHS可从美国CAP获得。
当前比较流行的特定蛋白的国际标准是CRM470,按照IFCC定值方案,统一使用指定的各特定蛋白纯化标准为原始标准。避免各实验室因使用的标准不一致造成定值差异。方案详细规定了定值的操作程序及统计方法。例如,为确保在检测时各标准、样品间无基体效应的差异和没有抗原过剩,要求回归线通过零点,标准和测定都须做多个稀释(须以重量法校正),每个稀释品做双份检测等。在1902年欧洲经济共同体参考局(BCR)认可该参考品,并给予代号CRM470(认可参考品CRM470)。
使用CRM470标准后,各重要厂商等已签署认可CRM470作为他们公司的第一标准,这带来了一系列的良好效果,如实验室结果的可比性得以改善;依赖方法偏差很低;任何时候任何人可以用;血清蛋白的化学物理特性很好;成年人参考范围的一致性;液体和尿液的分析也可以得到改善。
3.定标 定标是批特异性的。当试剂的批号更换时、更换特定部件时和保养程序后,试剂应该进行重新定标。免疫浊度分析仪设计为尽量减少定标次数,系统记忆保存的定标,可以通过每天检测中的质量控制的结果进行监控。定标有不同的稳定期。在定标过程中系统会自动完成确认检查,并提供定标报告。定标失败时系统会提醒操作者。
4.抗原过量的监测 由于免疫方法检测的特殊性,抗原过量的监测是检测结果质量控制的另一个重要保证。选择最优的方法学和专业的检测系统,是保证检测结果准确的首要前提。目前随着国内外对特定蛋白检测的重视,特别是更加有效的参考品的出现,有力地促进了特定蛋白检测质量水平的提高。
5.室内质量控制 认真做好室内质控工作,室内质量控制用于评估每个实验室的检测结果是否与以前相似,判定当日结果是否可以被采用。它控制着试验的重复性、精密度。借助于室内质控血清进行,每次检验常规标本时,同期进行质控血清检验,借助质控血清检验结果与原预定的可接受限相比较,不满意的结果将被控制。在特定维修或者出现故障后,都应该运行质控。根据工作量和工作流程,操作者自行判断是否更频繁地运行质控或使用附加质控品。
6.回顾性质控 目前多采用Westgard质控规则。它是回顾性的,可及时发现问题,总结偶然和必然误差发生的原因。Westgard质控规则是在Levey Jennings方法基础上发展起来,建立了同时使用多个规则来进行检验质量控制的方法,因此,很容易与常用的质控图进行比较并涵盖后者的结果,通过单值质控图进行简单的数据分析和显示;当失控时,能确定产生失控的分析误差的类型和误差范围,由此可帮助确定失控的原因以寻求解决问题的方法。通常有6个质控规则,即12S、13S、22S、 R4S、41S、10ˉx质控规则(图16-6)。
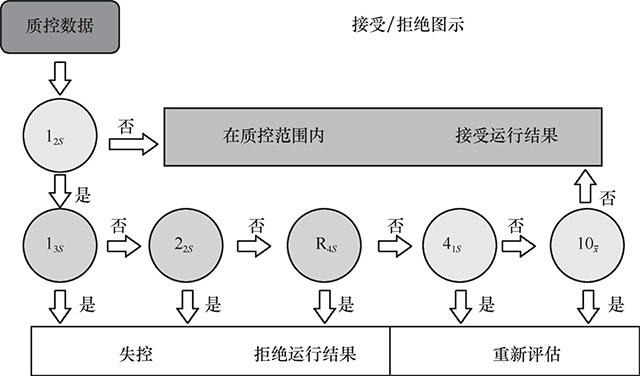
图16-6 Westgard质控规则运行示意
7.室间质控 做好室内质控的同时也要重视室间质控的作用。许多实验室之间比较某一样本的结果,确认同一样本,并给出一个正确的答案。室间质量评价提供准确度的评价,这是一个回顾性的评价,提供一个持续的检查该项目结果的可信度,使病人检验结果在不同医院之间可以通用。
室内质控的目的在于控制本室检测的精密度,使本实验室测定结果趋于稳定;室间质评目的是控制检验的准确度,使各实验之间结果具有可比性。两者相辅相成,缺一不可。
8.检测结果的准确性 检测结果应与临床相符,一旦出现异常结果,在排除实验室和人为因素后应及时与临床沟通,全面了解患者的病情以对结果作一正确评价。定期征求临床医师对检测结果的信息反馈,及时了解临床医师对检测项目的需求,更好地为患者服务。
(三) 运行结束后注意事项
仪器运行结束后应严格执行保养程序,这是保证仪器正常运行的根本。
(1) 每日保养:检查冲洗液余量及冲洗管道;检查废液桶及排废管道;必须没有阻碍;检查注射器阀、管道和活塞头;清洁试剂针、样品针、试剂搅拌针和样品搅拌针外表面。
(2) 每月保养:清洁仪器表面;清洁仪器所有风扇的过滤网;记录仪器工作次数。
(3) 特殊保养:清洁打印机打印头;对样品盘、试剂盘和样品架清洁及消毒;定时更换仪器使用部件如反应杯等。
(4) 特别注意事项:在仪器通电时不要拔插电路板,不要连接或断开管道的任何接头;对电路板操作时要戴防静电护腕;注意观察仪器保养的正确过程,安全操作;清洁仪器任何部件时要在仪器非工作状态下;在仪器启动和退出诊断程序时检查仪器所有机械部件;检查仪器底部有无液体渗漏。
 京公网安备11010102003307号
京公网安备11010102003307号

微信扫一扫
关注医隆网