本栏目由医隆网专家团队审核!
(一)色谱分析技术的发展
1.液相色谱( liquid chromatography,LC )分析技术的发展 液相色谱分析技术是20世纪早期由俄罗斯植物学家茨维特( Mikhail S. )提出的。 他最先尝试在装满颗粒的柱子上使用溶剂来分离从植物中提取的树叶色素。 随着样品由于重力自上而下流过柱子,可看到出现不同颜色的谱带,他将这些分开的不同颜色的谱带与样品中原有的不同化合物相关联,并提出使用色谱法( chromatography )来描述他的彩色试验。 现今,液相色谱法以各种形式表现,已成为分析化学中最有力的工具之一。
高效液相色谱( high performance liquid chromatography ,HPLC)又称为高压液相色谱,引自 Csaba Horváth 教授在1970年匹茨堡大会上的文章,原指在填料柱中产生所需的流速需要高压。 高压液相色谱分析技术早期只能承受500psi ( 1psi=6.895kPa )的压力,随着这一期间不断地改进性能,新型的高压液相色谱仪器可以承受 6000psi 的压力,并产生更小颗粒和更高压力,逐渐成为20世纪70年代中晚期的普遍分析方法。
高效液相色谱是目前分析化学最强大的工具之一,它能够分离、定性和定量任何可以溶解在液体中的化合物,甚至低至千万分之一(ppt)级别的痕量化合物也可以很容易地被鉴定出来。 高效液相色谱已经可以用于几乎任何一种样品的检测,如药品、食品、营养品、化妆品、环境物质、刑侦样品和工业化学品等。 2004 年,随着超高效液相色谱的推出,液相色谱设备和色谱柱技术取得了显著的进步,分离科学发生了革命性的变化,使得液相色谱的分离度、分离速度和灵敏度显著提高,帮助分析科学家取得了更多的成功,更大地提高了工作成效。
2.气相色谱(gas chromatography ,GC )分析技术的发展 气相色谱分析技术的发展到现在已经有上百年的历史,它是一种相当成熟且应用极为广泛的复杂混合物的分离分析方法。
20世纪初,被奉为色谱法创始人的俄国植物学家 Tswett 在1903年的华沙自然科学学会生物学会会议上,提出题目为“一种新型吸附现象及其在生化分析上的应用”的论文,叙述了应用吸附剂分离植物色素的新方法。 也是在这个报告中,“色谱”第一次被正式提出,这也标志着色谱的诞生。
到了20世纪40年代,英国人 Martin 和Synge在研究分配色谱理论的过程中,发现并证实了气体可以作为色谱运行载体的可行性,并且在后来发表了第一篇气相色谱相关的论文。 自此,气相色谱随着科学技术的不断进步,分析方法也得到了长足的发展,现在它发展成为影响最大、发展最快、应用最广泛的复杂混合物的现代分离分析方法之一。
历史上最早的气相色谱仪是1947 年由捷克色谱学家Jaroslav Janák 发明的 。1955 年首台商品化的气相色谱仪诞生。而作为气相色谱仪核心以色谱柱为代表的分离系统,其发展更为快速。 在气相色谱问世之初,色谱柱均为填充柱,由柱管及填装于柱管内的固定相组成。 填充柱制备简单、种类多、应用广泛,但由于样品负荷量大、柱渗透性较小、传质阻力较大、柱子不能过长等原因导致分离效率难以提高。 直到1979 年,Dandeneau 与 Zerenner 发明了弹性石英毛细管柱,它的优点是柔韧性好,不易断裂,且惰性内表面易于硅烷化后涂渍固定液,柱效很高,这是气相色谱领域的革命,从此色谱柱的发展得到质的飞跃。 20世纪80年代后,由于弹性石英毛细管柱的广泛应用,各种毛细管柱固定液应运而生,随后的数年中,固定液发展方向主要集中于选择性固定液,特别是分离对映异构体以及位置异构体的固定液。 随着电子技术的飞速发展,20世纪90年代出现了电子压力传感器和电子流量控制器,通过计算机实现压力和流量自动控制的电子程序压力流量控制系统,这是气路系统的一大进步,精准的控制能力使得方法的重现性和稳定性大幅提升,这可以称为是气相色谱发展史上的又一个里程碑。
到目前为止,气相色谱分析技术已经发展得相当成熟,在现代社会的方方面面,其均发挥着重要的作用,成为各种分离技术中效率最高和应用最广的手段。
(二)质谱分析技术的发展
1. 电感耦合等离子体质谱(inductively coupledplasma mass spectrometry,ICP-MS) 分析技术的发展 电感耦合等离子体质谱的历史可以追溯到20世纪80年代,由美国 Iowa 大学 Ames 实验室的 Houk 和Fassel 以及英国 Surrey 大学的 Gray 等人联名发表的“里程碑”文章。 而从第一篇文章的发表到第一台商品化的仪器问世仅3年的时间,1983年,加拿大 Sciex 公司和英国VG公司同时推出各自的第一代商品仪器 Elan 250 和 VG PlasmaQuad。 正是由于这些先驱者的不懈努力与合作,才使 ICP-MS 仪器能于20世纪80年代中期面市,并很快受到分析化学家及其他领域学者的青睐。 随着技术的成熟,ICP-MS已经由研究型仪器发展到了常规检测行列,它的应用领域已经从地质行业扩展到了环境、食品、医药、法医、半导体、材料等行业。
自20世纪90年代以来,ICP-MS的发展与应用更加快速,至今,仅中国已拥有近3000 台。 而且生产ICP-MS的厂家也由当时的两家(VG 公司后产品归入Thermofisher,Sciex此产品归入到PerkinElmer)扩大到十多家。 尽管各厂家所设计、生产的ICP-MS仪器的类型与某些工作特性,尤其是计算机控制系统及用户界面均有差异,但在近30来年的发展历程中,在ICP-MS基础研究与应用研究的支持下,其不断完善与更新,使之越来越受到用户的欢迎。
2. 气相色谱-质谱联用( gas chromatography mass speceromrtry,GC-MS) 分析技术的发展 GC-MS是分析仪器中较早实现联用技术的仪器。 自1957年霍姆斯( J.C.Holmes ) 和莫雷尔(P.A.Morrell )首次实现气相色谱和质谱联用以后,这一技术得到长足的发展。 在所有联用技术中,GC-MS发展最完善,应用最广泛。 目前从事有机物分析的实验室几乎都把GC-MS作为主要的定性确认手段之一,在很多情况下又用GC-MS进行定量分析。 GC-MS逐步成为分析复杂混合物最为有效的手段之一。
为了应对复杂基质中多成分同时分析在样品前处理方法开发和自动化等方面的需求,同时为了使操作更简便、装置完全自动化、减小误差等目的,样品前处理的自动简便在线联用系统实现了与气质联用仪的很好连接使用。 而对于组分非常复杂的样品,当单一色谱柱对化合物的分析变得很困难的时候,可以采用多维气相色谱技术,利用两根不同极性的色谱柱,在一根色谱柱上无法完全分离的组分,可导入第二根色谱柱进一步分离,从而使复杂组分的分离成为可能。
1991年最先使用的全二维气相色谱( GC×GC ),不同于通常的二维色谱( GC+GC ),它是把分离机理不同而又互相独立的两支色谱柱以串联方式结合成二维气相色谱,在这两支色谱柱之间装有一个调制器,起捕集再传送的作用。 经第一根色谱柱分离后的每一个馏分,都需先进入调制器,进行聚焦后再以脉冲方式送到第二根色谱柱进行进一步的分离。 所有组分从第二根色谱柱进入检测器,信号经数据处理系统处理,得到以柱1保留时间为第一横坐标,柱2保留时间为第二横坐标,信号强度为纵坐标的三维色谱图或二维轮廓图。 使用全二维气相色谱容易解决干扰问题,分析速度也得以加速。
3.液相色谱-串联质谱( liquid chromatography mass spectrometry,LC-MS ) 分析技术的发展 LC-MS技术的研究始于20世纪70 年代,同GC-MS较早即成熟并投入大规模应用不同,液质联用的发展经历了一个更长的发展过程。90年代以来,由于大气压电离的成功应用以及质谱技术本身的发展,液相色谱与质谱的联用,尤其是液相色谱与串联质谱的联用得到了快速的发展。
早期的质谱主要用来测定同位素和无机元素,20世纪40年代以后,质谱仪开始应用于有机质谱分析,60 年代出现了气相色谱-质谱联用仪,使质谱仪的应用领域大幅扩展,开始成为有机物分析的重要仪器。 80年代以后出现的新电离技术使得质谱分析技术又取得了长足的进展,现在 LC-MS/MS 法已经是临床分析非常重要的常用分析方法。
虽然自20世纪70年代初,科学家们就开始致力于液质联用接口技术的研究。 但在开始的20年中处于缓慢的发展阶段,曾出现了许多种联用接口,这些接口技术均有自己的开发完善过程,都有自己的长处和缺点,有的仅仅在某些有限的领域和范围内被使用,但受制于各种各样的技术问题,这些接口均没有应用于商业化生产。 直到大气压离子化( atmospheric-pressure ionization, API )接口技术的问世,液质联用才得到迅猛发展,API接口技术是非常实用和高效的“软”电离技术,是质谱技术的重大突破,广泛应用于实验室内分析和各个应用领域。 API 接口技术是当今世界上几乎每台质谱都在使用的接口技术。 而首创于1988年的基质辅助激光解吸电离(MALDI)离子化方法同电喷雾(ESI)离子化方法一起,更是使质谱飞跃出传统物理学、化学进入生物学分析的领域。
4.基质辅助激光解吸电离飞行时间质谱(matrix assisted laser desorption lonization time of flight mass sprctrometry ,MALSI-TOF)分析技术的发展 质谱的开发历史要追溯到20 世纪初 J.J.Thomson 创制的抛物线质谱装置,从世界上第一台质谱仪问世到现在已有100多年了,早期的质谱仪主要是用来进行同位素测定和无机元素分析,随着离子光学理论的发展,质谱仪不断改进,其应用范围也在不断扩大。 20世纪80年代以后开始出现了一些新的质谱技术,如快原子轰击电离子源,基质辅助激光解吸电离源,电喷雾电离源,大气压化学电离源,以及随之而来的比较成熟的液相色谱-质谱联用仪,感应耦合等离子体质谱仪,傅里叶变换质谱仪等。 这些新的电离技术和新的质谱仪的出现使质谱分析取得了长足进展。 质谱技术在生命科学领域的应用,更为质谱的发展注入了新的活力,形成了独特的生物质谱技术。
1886 年,Goldstein发现正电荷离子;
1898 年,Wien 利用电场和磁场使正电荷离子偏转;
1912年,Thomson 研制世界上第一台质谱仪,氖同位素的发现;
1918 年,Dempster发现电子轰击电离及磁聚焦;
1919 年,Aston 发明精密仪器,测定50多种同位素,第一张同位素表问世;
1934 年,Stephens 发现均匀扇形磁场;
1940 年, Nier 发明扇形磁场偏转质谱计;
1946 年,Stephens 发明飞行时间质谱( time-offlight mass analysis );
1953 年,Paul 等发明四极杆分析器( quadrupoleanalyzers );
1965 年,Hipple 等发明离子回旋共振( ion cy-clotron resonance );
1966 年,Munson 和 Field 发明化学电离(chemical ionization);
1966 年,McLafferty 和 Jennings 发明串联质谱( tandem mass spectrometry );
1974 年,Comisarow 和 Marshall 发明傅里叶变换离子回旋共振质谱;
1981年,Barber 等发明快原子轰击电离质谱;
1989 年, J.B.Fenn发现电喷雾电离;Koichi Tanaka 发现基质辅助激光解吸电离;
1990 年,Katta 和 Chait 通过电喷雾电离质谱观察蛋白质构象改变;
1993 年,商品化电喷雾质谱仪问世;
1995 年,傅里叶变换离子回旋共振质谱仪问世;
1998 年,高分辨率飞行时间质谱仪问世;
2002 年,J.B.Penn 和田中耕因电喷雾电离( electron spray ionization,ESI )质谱和基质辅助激光解吸电离(matrix-assisted laser desorption ionization ,MALDI)质谱获诺贝尔化学奖。
近年来,全球质谱仪市场增长快速,预计2017年全球质谱技术市场容量将达到48.4亿美元。其在制药、化工、食品、环境等方面已经是主力军,在临床检测方面的市场需求也在逐步打开。目前,质谱仪器正向更高效率、小型化发展,出现便携式质谱仪。一些仪器联用技术如GC-MC、HPLC-MS、GC-MS-MS、ICP-MS等正大行其道。无论是质谱技术人员,还是质谱仪生产厂商都已看到这个巨大需求市场,都在积极进行研究与开发,涉及便携质谱仪制造的一些关键技术已经常熟,现在正处于从大型质谱仪向小型质谱仪转型的时期。
1.液相色谱(liquid chromatography ,LC)分析技术的分类
高效液相色谱是目前分析化学最强大的工具之一,它能够分离、定性和定量任何可以溶解在液体中的化合物。 每一个化合物在一个特定的位置,保留时间(tR)计算从进样到峰最高点洗脱出来为止。 比较每个峰的保留时间和相同流动相、固定相的色谱系统标准物质的保留时间,就可能鉴定每一个化合物。 色谱图和相应数据给出化合物的含量帮助我们计算每种化合物的浓度。 色谱图基本上反映化合物通过流通池的浓度,浓度越高,信号越强,这可从基线上色谱峰高度观察到。
高效液相色谱除了可以用于定性和定量样品中的化合物,也可以用来纯化和收集所需的每一个化合物,在流通池下游使用组分收集器。 这个过程被称为制备液相。 在制备液相中,可以收集每个流出色谱柱的组分。 馏分收集器在特定的时间段,选择收集纯化了的组分。 收集瓶可移动,从而使每瓶只收集单个峰的组分。 总的来说,随着样品量的增加,高效液相色谱柱尺寸将会加大,泵也会需要更高的体积流速。
总的来说,根据化合物的三种主要的性质可以进行高效液相色谱分离,分别是化合物极性、电荷、分子大小。
(1) 基于极性的分离:分子的结构、活性和物理化学性质由它的原子和化学键决定。 在一个分子内部,决定了其特殊性质和可预测的化学反应的特定排列,称为官能团。 这个结构经常决定这个分子是极性还是非极性。 有机分子根据它含有的主要官能团来分类。 基于极性的分离模式,不同分子的相对色谱保留时间大都由这些官能团的性质和位置决定。 例如,水具有强偶极矩是极性化合物,苯是芳香族碳水化合物,是非极性化合物。 具有相似色谱极性的分子相互吸引,如果极性不同相互的吸引力会减弱,极端的情况是相互排斥。 这是基于极性的色谱分离模式的基本原理。 通过选择流动相和固定相制造样品中各种化合物的竞争。 这样,样品中和固定相极性相似的化合物将被延迟因为它们更强地被颗粒吸引。 而和流动相极性相似的化合物将优先被吸引而移动较快。同性相吸的原则将决定哪一种分析物洗脱速度慢,哪一种洗脱速度更快。
1)正相高效液相色谱 在植物提取物的分离过程中,茨维特成功运用极性固定相和弱极性流动相。 这种经典的色谱模式被称为正相。 在进行正相色谱分离时,极性强的化合物被保留在极性的固定相。 相对的非极性的化合物在非极性溶剂的流动相作用下很快被洗脱出来。 对硅胶柱正相色谱来说,典型的情况流动相是100% 有机相,不含水。
2) 反相高效液相色谱 反相是指与正相恰好相反的色谱模式,使用极性流动相和非极性固定相。 最强保留的化合物是非极性较强的化合物,因为它与非极性的固定相吸附最强。 极性的化合物,较弱保留,在极性水性流动相的作用下,流过填料最快,最早被洗脱出来。 今天,由于反相色谱有更好的重现性和更广泛的应用,反相色谱占所有高效液相色谱方法的75% 。 大多数方法使用水和极性溶剂的混合物,如甲醇或乙腈。 这样一般来说能保证分析物与非极性,疏水性颗粒表面的适当相互作用。 目前,键合硅胶是最普遍的反相高效液相色谱柱填料。
3)亲水作用色谱(HILIC) 亲水作用色谱可以看作是正相色谱的一种变化。 正相色谱中,流动相是百分之百有机相。 只有痕量水分存在于流动相和极性填料的空隙里。 极性分析物与极性固定相吸附较强,不会被洗脱下来。
在有机流动相如乙腈中加入一些水分(<20% ),就可能分离和洗脱在正相模式下强保留或反相模式下弱保留的极性化合物。 水是强极性溶剂,和极性分析物有效竞争固定相。 亲水作用色谱HILIC 可以在等度或梯度洗脱模式下运行。 随着流动相极性的增加,最初吸附在极性填料颗粒的极性化合物可以被洗脱下来。 分析物按照亲水性由低至高的顺序被洗脱出来。 缓冲液或盐可加至流动相中以保持离子化的分析物呈单一形式。
4)疏水作用色谱(HIC) 疏水作用色谱是一种反相色谱用来分离大的生物分子,如蛋白。 这些分子通常为保持原形而置于水溶液中,避免和会使其变性的有机溶剂或表面活性剂接触。 HIC通过疏水性固定相来达到大分子疏水目的,例如,适用 硅胶柱。 在起始阶段,水中高盐浓度将帮助填料保留蛋白。 梯度分离经常是通过递减盐浓度来进行。这样,生物分子按照疏水性由低到高被洗脱出来。
(2) 基于电荷的分离———离子交换色谱(IEC):基于极性的分离,即同性相吸,异性相斥。而基于电荷的离子交换色谱规则是相反的,即同性相斥,异性相吸。 离子交换分离的固定相以表面酸碱性强弱和吸附保留的离子类型来划分。 阳离子交换是用负电荷表面来保留和分离带正电荷的离子。 反之亦然,阴离子交换是用正电荷表面来保留和分离带负电荷的离子。 每一种离子交换类型,都至少有两种分离和洗脱方法。
强离子交换体系指具有易离子化的官能团季胺类或磺酸类。 它们主要用于保留和分离弱离子。这些弱离子可以被能更强吸附在固定相表面的流动相洗脱或代替。 或者,弱离子可以被保留在柱上,之后通过原位改变流动相的PH被中和,使其失去吸附力而被洗脱。
弱离子交换体系指二胺类或羧酸类,可在某个PH 以上或以下被中和而失去保留带电离子的能力。 当带电荷时,它们用来保留和分离强离子。 如果这些离子不能被替代物洗脱,可以用中和固定相的方法消除离子化吸附,使得带电分析物被洗脱下来。 当弱离子交换体系被中和,它们可以通过反相或正相相互作用保留和分离化合物,在这样的情况下,洗脱强度由流动相的极性来决定。 因此,弱离子交换体系可用于基于极性和电荷的混合分离模式(图12-23)。
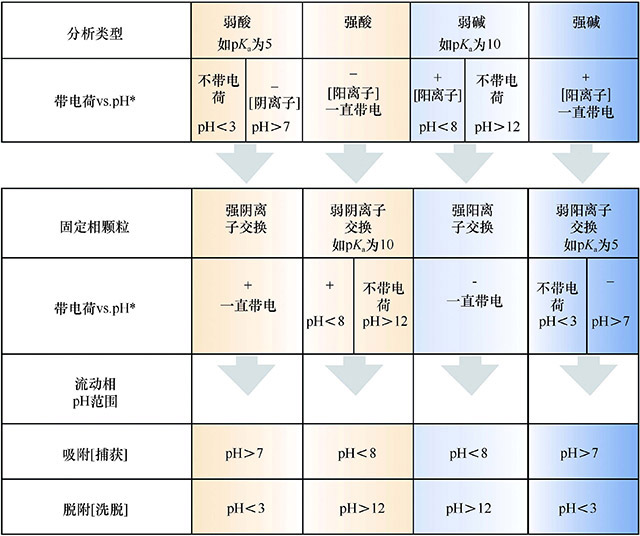
图12-23 离子交换分类
提示:PH 的范围是粗略的,这与特定的分析物和颗粒的特征有关。
离子交换色谱不适用强-阳离子交换体系保留强碱物质,两者都带电荷并强烈地相互吸引,使得碱性物质几乎无法洗脱出来。 只能用更强保留的竞争型碱物质来冲洗这个强阳离子交换体系,替换目标化合物。 这种做法在高效液相色谱和固相萃取几乎没有实用性,也不安全。
(3)基于尺寸大小的分离:排阻色谱(SEC)-凝胶渗透色谱(GPC):19 世纪50 年代,Porath 和Flodin 发现生物分子通过过滤或流经孔径可控的亲水右旋糖苷聚合物时可以按照分子大小被分开。这个过程被称为凝胶过滤。 后来,一种类似的装置,使用特定孔径范围的有机聚合物填料分离合成寡聚物和多聚物,这个过程称为凝胶渗透色谱(GPC)。 使用孔径可控的硅胶填料类似的分离过程被称作排阻色谱(SEC世界上第一台用于GPC的商业化高效液相色谱仪出现在1963年。
这些技术通常是通过固定相来实现。 固定相是合成的有一定孔径分布的填料,使得感兴趣的分析物进入或不能进入孔内来实现分离。 小分子在通过填料床时更多地进入到颗粒孔隙中。 大分子只能进入某一尺寸以上的孔隙,在填料床停留的时间较短。 最大的分子可能完全不能进入孔内而只在颗粒间通过,因此被流动相很快洗脱出来。 这里选择流动相有两个条件:第一,对被分析物来说是良好的溶剂;第二,可以防止被分析物和固定相表面的相互作用。 这样,大分子先洗脱出来,小分子因为进入更多的孔,流动慢后洗脱出来,按照在溶液中的尺寸由高至低的顺序。 因此,简单的规则是大的先出来。
(4)超高效液相色谱:2004 年,随着超高效液相色谱的推出,分离科学发生了革命性的变化。 在色谱设备和色谱柱技术上取得了显著的进步,使得液相色谱的分离度、分离速度和灵敏度显著提高,实现超高速分析,超高分离度。
为了使分离性能最大化,不仅仅需要考虑小的填料和较高的压力。 为了实现2μm 颗粒柱的色谱效益,这些色谱柱必须在特别设计的色谱仪上使用,以耐受较小颗粒所产生的压力,同时通过将色谱柱内、柱外谱带展宽的最小化。 常规HPLC系统不能实现这一点。 UHPLC系统全面考虑了色谱和色谱柱的所有方面,通过整体化的设计途径,提高色谱分离的性能和分析数据的质量。
2.气相色谱(gas chromatography,GC)分析技术的分类
气相色谱的核心是色谱柱,它是实现混合组分分离的基石,根据所配置色谱柱的不同,气相色谱可以分为几类,常见的气相色谱的分类方法也有几种。
(1)按色谱柱分类:可分为填充柱气相色谱和开管柱气相色谱。 填充柱内要填上一定的填料,是“实心”的,而开管柱则是“空心”的,它的固定相是涂覆在管柱内壁上的。 在气相色谱的发展史上,早期都以填充柱为主,直到1958年才出现了开管柱,而开管柱的广泛使用则是在惠普于1979 年研发出的首款弹性石英柱后才开始的。
(2)按固定相状态分类:可分为气固色谱和气液色谱。 前者采用的固定相为固体,如多孔氧化铝或高分子小球等,主要应用于永久气体和较低分子量化合物的分离,其分离的基本原理是吸附。 后者所采用的固定相为液体,是气相色谱中应用最为广泛的类型,其分离主要是基于分配机制。
(3)按进样方式分类:可分为常规色谱、顶空色谱和裂解色谱等。
气相色谱可以分析的样品范围极为广泛,从石油化工、环境保护,到食品分析、医药卫生,气相色谱都发挥着重要的作用。 其中,在医药分析中的主要应用包括雌三醇的测定、尿中孕二醇和孕三醇的测定、尿中胆甾醇的测定、儿茶酚胺代谢产物的分析、血液中乙醇、麻醉剂以及氨基酸衍生物分析、血浆中睾丸激素分析、某些挥发性药物分析等。
3.电感耦合等离子体质谱(inductively coupledplasma mass spectrometry ,ICP-MS)分析技术的分类
ICP-MS是化学元素分析领域独一无二的卓越仪器。 元素周期表上的大多数元素无论是主量元素、少量元素还是痕量元素,其在各种类型样品中的含量几乎都可以用ICP-MS来检测。 除了液体中元素分析以外,ICP-MS还可以偶联激光剥蚀设备从而直接分析固体样品中的化学元素含量;也可以与HPLC 或GC 联用,对特定元素进行形态分析。
4.气相色谱-质谱联用( gas chromatography mass spectrometry ,GC-MS)分析技术的分类
1) 按色谱柱的结构分类:可分为填充柱和开管柱。 填充柱中间填充了填料作为固定相,看上去是实心的ꎻ而开管柱的中间没有填料,其固定相是涂敷在管壁的,所以看上去是空心的。 虽然开管柱又常被称为毛细管柱,但毛细管柱并不总是开管柱。事实上,毛细管柱也有填充型和开管型之分,只是人们习惯上将开管柱叫做毛细管柱而已。 本章除特别说明外,都用毛细管柱来指开管柱。
毛细管柱比填充柱有更高的分离效率,这是因为毛细管柱内没有固体填料,气阻比填充柱小得多,故可采用较长的柱管和较小的柱内径,以及较高的载气流速。 这样,既消除了填充柱中涡流扩散的问题,又大大减小了纵向扩散造成的谱带展宽。而采用较薄的固定液膜又在一定程度上抵消了由于载气流速增大而引起的传质阻力增大。 一般来说,一根30m 长的毛细管柱很容易达到100 000的总理论塔板数,而一根3m 长的填充柱却最多只有4500的总柱效。
但是,毛细管柱也有其局限性。 因为其内径小,所以容量小,且对进样技术的要求更高,载气流速的控制要求更为精确。 进样量过大很容易造成柱超载,因而要求检测器的灵敏度更高。 一般来讲,填充柱的可接受的单个组分是微克量级,而毛细管柱则只能承受纳克量级。
2) 按固定相状态分类:按固定相状态分可分为气固色谱和气液色谱。 前者采用固体固定相,如多孔氧化铝或高分子小球等,主要用于分离永久气体和较低分子量的有机化合物,其分离主要是基于吸附机理。 后者则为液体固定相,分离主要基于分配机理。 在实际GC分析中,90% 以上的应用为气液色谱。
3) 按分离机理分类:按分离机理可分为分配色谱(即气液色谱)和吸附色谱(即气固色谱)。 应当指出,气液色谱并不总是纯粹的分配色谱,气固色谱也不完全是吸附色谱。 一个色谱过程常常是两种或多种机制的结合,只是有一种机制起主导作用而已。
4) 按进样方式分类:按进样方式分可分为常规色谱、顶空色谱和裂解色谱等。除了上面所述,还有一种特殊的GC 类型,叫逆相色谱,又叫反相色谱。 它是将欲研究的对象作为固定相,而用一些有机化合物(叫探针分子)作为样品进行分析。 目的是研究固定相与探针分子之间的相互作用。 比如在高分子领域,用此法研究聚合物与有机化合物的相互作用参数。
气质联用的质谱仪根据所用质量分析器的原理,可以分为:磁质谱、离子阱质谱(IT)、四极杆质谱(Q)、飞行时间质谱(TOF)、傅里叶变换质谱(FT-MS),以及多个质量分析器联用形成的串联质谱,如三级四极杆质谱、Q-TOF等。
5.液相色谱-串联质谱(liquid chromatography mass spectrometry , LC-MS)分析技术的分类
LC-MS根据接口不同, 可分为以下三种技术:
(1) 电喷雾离子化技术:电喷雾(ESI)技术作为质谱的一种进样方法起源于20世纪60年代末Dole等的研究,直到1984 年Fenn 实验组对这一技术的研究取得了突破性进展。 1985 年,科学家们将电喷雾进样与大气压离子源成功连接。 1987 年,Bruins等发展了空气压辅助电喷雾接口,解决了流量限制问题,同时可以在常温常压下实现离子化过程,同时对热不稳定性化合物、肽、蛋白质、核酸等生物大分子进行分析,当时即引起世界性轰动。 随后第一台商业化生产的带有API源的LC-MS联用仪API Ⅲ于1989 年问世。ESI的大发展主要源自于使用电喷雾离子化蛋白质的多电荷离子在四极杆仪器上分析大分子蛋白质,大大拓宽了分析化合物的分子量范围。2002年Fenn 因为对电喷雾质谱技术的贡献获得了诺贝尔化学奖。
该种离子化方式是目前为止最软、最温和的离子化方式。 ESI源主要由五部分组成:液体导入装置、大气压离子化区域、离子取样孔、大气压到真空的界面、离子光学系统。 电喷雾过程可被分为液滴形成、液滴挥发和气态离子形成。 在ESI方式下,离子的形成是分析物分子在带电液滴的不断收缩过程中发生库仑爆炸产生的,即离子化过程是在液态下完成的。 液相色谱的流动相流入离子源,在氮气流及强电场下被雾化为带电的液滴,带电液滴不断挥发,体积不断缩小,强电场形成的库仑爆炸使小液滴样品离子化,离子表面的液体借助于逆流加热的氮气分子进一步蒸发,使分子离子相互排斥形成微小分子离子颗粒。 由于产生的单一分子形式的气态离子可能有几种电荷态,并且在接口中经历离子分子碰撞,还可能导致气态离子电荷态的变化,这样通常会观察到多重电荷形式,这一特点对于蛋白及多肽的分析至关重要。 电喷雾离子化的原理示意见图12-24。
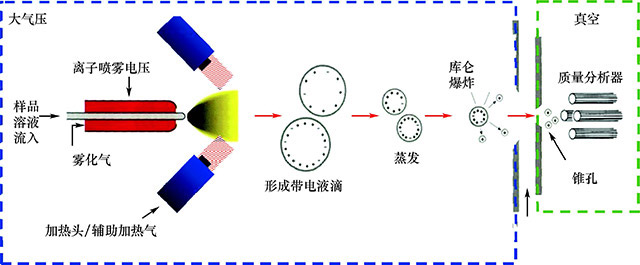
图12-24 电喷雾离子化原理示意
电喷雾离子化技术的突出特点:适用范围广,可以生成高度带电的离子而不发生碎裂,可将质荷比降低到各种不同类型的质量分析器都能检测的程度,通过检测带电状态可计算离子的真实分子量,同时,解析分子离子的同位素峰也可确定带电数和分子量。 另外,ESI 可以很方便地与其他分离技术联接,如液相色谱、毛细管电泳等,可方便地纯化样品用于质谱分析。 因此在临床分析、药物残留、药物代谢、蛋白质分析、分子生物学研究等诸多方面得到广泛的应用。 其主要优点:离子化效率高,离子化模式多,正负离子模式均可以分析,对蛋白质的分析分子量测定范围高达十万以上,对热不稳定化合物能够产生高丰度的分子离子峰,可与大流量的液相直接联机使用。
(2) 大气压化学离子化及大气压光电离技术:大气压化学离子化(APCI技术应用于液质联用仪是由Horning等于20 世纪70年代初发明的,直到20世纪80年代末才真正得到突飞猛进的发展,与ESI源的发展基本上是同步的。 但是APCI技术不同于传统的化学电离接口,它是借助于电晕放电启动一系列气相反应以完成离子化过程,因此也称为放电电离或等离子电离。 从液相色谱流出的流动相进入具有雾化气套管的毛细管,被氮气流雾化,
通过加热管时被汽化。 在加热管端进行电晕尖端放电,溶剂分子被电离,充当反应气,与样品气态分子碰撞,经过复杂的反应后生成准分子离子。 整个电离过程是在大气压条件下完成的(图12-25)。
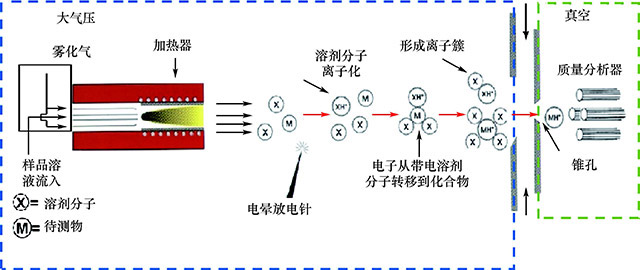
图12-25 大气压化学离子化原理示意
APCI 的优点:这是一种非常耐用的离子化技术,与ESI 相比,对溶剂类型、流速和流动相添加剂的依赖性较小,适合于非酸非碱性,且对蒸发、溶剂、流速、添加物等条件敏感的样品的分析。 它不受大部分条件微小变化的影响,因此非常易用和耐用。 APCI离子化方式适用于中等极性到弱极性的化合物分析,形成的是单电荷的准分子离子,不会发生ESI过程中因形成多电荷离子而发生信号重叠、降低图谱清晰度的问题;APCI离子化源可以适应高流量的梯度洗脱的流动相;采用电晕放电使流动相离子化,能大大增加离子与样品分子的碰撞频率。
ESI 与APCI 两种接口的电离方式在结构上有很多相似之处,但也有不同的地方。 掌握它们的差异对正确选择不同电离方式用于不同样品的分子量测定与结构分析具有重要的意义。 它们的主要差别:
1) 电离机理:电喷雾采用离子蒸发方式使样品分子电离,而APCI电离是放电尖端高压放电促使溶剂和其他反应物电离、碰撞及电荷转移等方式形成了反应气等离子区,样品分子通过等离子区时,发生了质子转移而生成[M+H]+或[M-H]-。
2) 断裂程度:APCI 源的探头处于高温,尽管热能主要用于汽化溶剂与加热N2气,对样品影响并不大,但对热不稳定的化合物就足以使其分解,产生碎片,而电喷雾源探头处于常温,所以常生成分子离子峰,不易产生碎片。
3) 灵敏度:APCI 与ESI 源都能分析许多样品,而且灵敏度相似,很难说出哪一种更合适。 同时至今没有一个确切的准则判断何时使用某一种电离方式更好。 但是通常认为电喷雾有利于分析生物大分子及其他分子量大的化合物,而APCI 更适合于分析极性较小的化合物。
4) 多电荷:APCI 源不能生成一系列多电荷离子,所以不适合分析生物大分子。 而ESI源特别适合于蛋白质,多肽类的生物分子,由于它能产生一系列的多电荷离子。
(3) 大气压光电离子化技术(APPI):是一种被分析物在气相中吸收由真空-紫外灯(V-UV lamp)发出的光子(10eV 或10.6eV)后放出电子从而离子化的过程。 该能级能量足够高,可以离子化很多的有机化合物但是将空气和常见的液相色谱流动相(如甲醇、乙腈和水)的离子化减至最低。 与ESI 和APCI相比, APPI 直接将待测物电离,所以它不局限于气相、酸碱化学的原理。 而且大气压光电离(APPI)源可以将其他大气压离子化技术无法电离的化合物离子化。LC-APPI-MS 在药物及其代谢物分析、环境分析、天然产物分析及有机合成等领域均有一定的应用,但LC-APPI-MS 比较适合非极性或弱极性化合物的分析,如镇痛药、脂溶性维生素、多环芳烃、杀虫剂、脂肪酸、类脂和甾体激素等。 这与APCI 有所重叠,但可测定APCI 不可准确测定的极端非极性化合物。 但是总体来说,限于APPI源擅长测试非极性及弱极性化合物的特点,这种源目前更多应用在环境等研究领域。
上述三种API源各自的适用范围,可以参考图12-26。
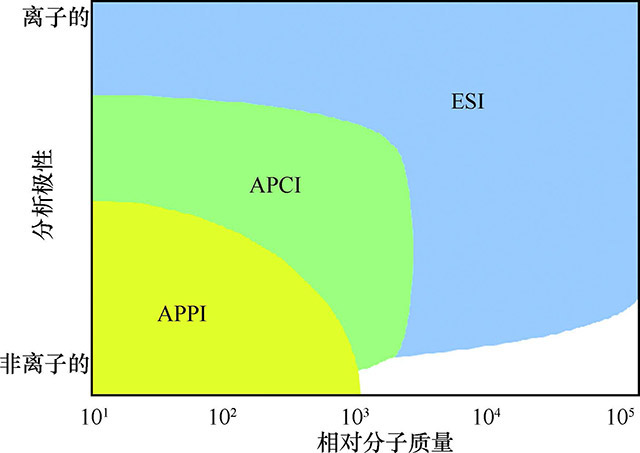
图12-26 ESI、APCI、APPI 三种离子化方式的适用范围
(一) 液相色谱分析技术质量标准
根据 JJG705-2014《液相色谱仪检定规程》,液相色谱仪的主要检定项目有输液系统、柱温箱、检测器和整机。其中输液系统包括泵压力、泵流量设定值误差SS、泵流量稳定性SR 和梯度误差Gi 的检定。柱温箱包括温度设定值误差△TS 和温度稳定性TC的检定。检测器包括基线噪声、基线漂移、最小检测浓度、波长示值误差和重复性与线性范围的检定。整机包括定性重复性检定和定量重复性的检定。具体计量性能要求如下:
1. 输液系统
(1) 输液管路接口紧密牢固,在规定的压力范围内无泄漏。
(2) 泵流量设定值误差SS 和流量稳定性SR 应符合表12-10的要求。
(3) 梯度最大允许误差Gi:±3% (见下表)。
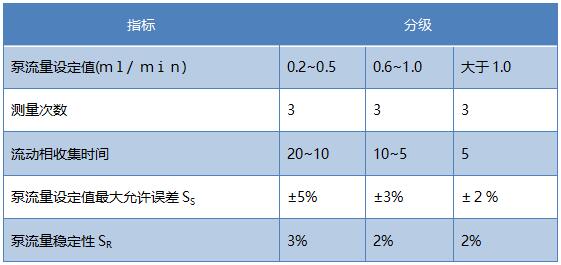
注:①最大流量的设定值可根据用户使用情况而定;②对特殊的、流量小的仪器,流量的设定可根据用户使用情况选大、中、小三个流量,流动相的收集时间则根据情况适当缩短或延长。
2. 柱温箱
(1) 柱温箱设定值最大允许误差:±2℃。
(2) 柱温箱温度稳定性:≤1℃ / h。
3. 检测器 仪器的检测器的主要技术指标见表12-11。
表12-11 液相色谱仪检测器的主要技术指标
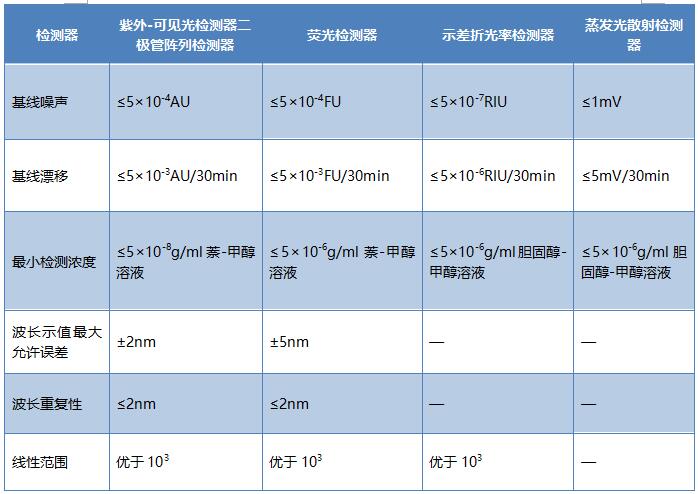
注:若仪器的输出信号用mV 或V表示,注意查看仪器说明书或仪器标牌表明的其与AU(FU)的换算关系:若无特殊表明通常可按照1V=1AU(FU)进行换算。
4.整机性能 仪器的整机性能用定性定量测量重复性表示,指标要求见表12-12。
表12-12 液相色谱仪整机性能指标要求
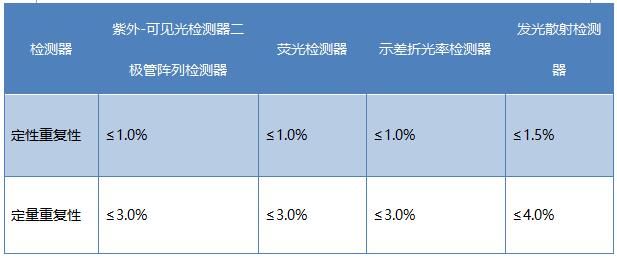
部分高效液相色谱卫生行业标准:
《尿中2-硫代噻唑烷-4-羧酸的高效液相色谱测定方法》( WS/ T40-1996 );
《血清肌酐测定参考方法同位素稀释液相色谱串联质谱法》( WS/T413-2013 );
《尿中肌酐的反相高效液相色谱测定方法》( WS/T98-1996 );
《尿中马尿酸、甲基马尿酸的高效液相色谱测定方法》( WS/T53-1996 );
《尿中五氯酚的高效液相色谱测定方法》( WS/T61-1996 );
《尿中苯乙醛酸和苯乙醇酸的高效液相色谱测定方法》( WS/T54-1996 );
《尿中对硝基酚的高效液相色谱测定方法》( WS/T58-1996 );
《尿中对氨基酚的高效液相色谱测定方法》(WS/T56-1996)。
(二) 气相色谱分析技术质量标准
就国内计量检定而言,气相色谱仪检定装置根据《气相色谱仪检定规程》(JJG 700-1999)所提供的方法,气相色谱仪的主要检定项目是载气流速稳定性检定、温度检定和检测器性能的检定三大项,温度检定又分为柱箱温度稳定性的检定和程序升温重复性的检定,而检测器性能的检定又分为基线噪声和基线漂移的检定、灵敏度或检测限的检定和定量重复性的检定。
(1) 计量标准的组成:国内的计量标准装置由载气流量计、气相色谱仪检定测量仪、气相色谱仪检定用标准物质等组成。
(2) 载气流速稳定性检定:用载气流量计对载气流速稳定性进行检定。
(3) 温度检定:用气相色谱检定测量仪温度信号输出的变化来对柱箱温度进行稳定性检定和程序升温重复性检定。
(4) 检测器性能检定
1) 基线噪声和基线漂移检定。 待基线稳定后,根据输出信号进行基线噪声和基线漂移的检定。
2) 灵敏度或检测限的检定。 用气相色谱仪检定用标准溶液来对检测器进行检定,根据信号输出的峰高或峰面积来对灵敏度或检测限进行计算。
3) 定量重复性的检定。 方法及所用标准物质同灵敏度或检测限的检定。
仪器的设计和制造商通过ISO 9001质量体系认证,生产的产品可参考下列标准执行。 电磁兼容性标准,包括欧盟电磁兼容性规范;安全性标准,包括欧盟低压规范;国际电工委员会标准(IEC);加拿大标准委员会标准(CSA);欧洲标准化委员会标准;中国计量器具认证;澳大利亚电磁兼容性标准。
针对气相色谱在临床的应用,还有一些发布的标准、规范可供参考:
《溶剂残留的检测》(中国药典2010 版);
《附录IXQ 农药残留测定法》 ( 中国药典2010 版);
《医用输液、输血、注射器具检验方法第1部分: 化学分析方法》(GBT 14233.1-2008);
《一次性使用医疗用品卫生标准》(GB 15980-2009);
《血中乙醇的气相色谱测定方法》 ( 地方标准DB34T 580-2006 );
《呼出气中丙酮的气相色谱测定方法》(卫生行业标准WST 175-1999);
《呼出气中二硫化碳的气相色谱测定方法》(卫生行业标准WST 41-1996 );
《尿中苯酚的气相色谱测定方法(一) 液晶柱法》(卫生行业标准WST 49-1996);
《尿中苯酚的气相色谱测定方法(二) FFAP 柱法》(卫生行业标准WST 50-1996 );
《呼出气中苯的气相色谱测定方法》( 卫生行业标准WST51-1996 );
《尿中4-氨基-2,6-二硝基甲苯的气相色谱测定方法》卫生行业标准WST 59-1996);
《尿中甲醇的顶空气相色谱测定方法》(卫生行业标准WST 62-1996 );
《尿中亚硫基二乙酸的气相色谱测定方法》(卫生行业标准WST 63-1996 );
《疑似毒品中甲基苯丙胺的气相色谱、高效液相色谱和气相色谱-质谱检验方法》(国家标准GBT 29636-2013 );
《疑似毒品中氯胺酮的气相色谱、气相色谱-质谱检验方法》(国家标GBT 29637-2013);
《生物样品中g-羟基丁酸的气相色谱-质谱和液相色谱-串联质谱检验方法》 (公共安全行业标准GA/T1074-2013);
《台式气相色谱-质谱联用仪校准规范》(国家计量技术规范 JJF 1164-2006)。
(三) ICP-MS 质量标准
ICP-MS 仪器性能检定可按照国家质量监督检验检疫总局批准的《四极杆电感耦合等离子体质谱仪校准规范》(JJG 1159-2006)进行。 其规定了四极杆ICP-MS校准项目和技术指标:
(1) 背景噪声:指未引入某元素离子时,质谱检测系统产生的该元素离子信号响应。
(2) 检出限:质谱仪所能测定的某元素的最低极限质量浓度。 表示方法为空白溶液中某元素的n次测量结果的3倍标准偏差所对应的质量浓度。
(3) 灵敏度:单位浓度的元素在质谱仪检测器上得到的信号响应(技术),单位Mcps/mg。
(4) 丰度灵敏度:表征某一质量为M的强离子峰在相邻质量M+1(或M-1)位置上的前峰或拖尾峰对相邻峰的影响。
(5) 氧化物离子产率:某元素原子在等离子体中电离时生成氧化物离子与该元素的单电荷离子的比。
(6) 双电荷离子产率:某元素原子在等离子体中电离时生成双电荷离子与该元素的单电荷离子的比。
(7) 质量稳定性:表示在较长时间内某元素的质量峰中心偏移的程度。
(8) 分辨率:以元素质量峰高10% 处的峰宽度表示。
( 9) 冲洗时间:是指用稀硝酸将仪器中某元素的信号强度冲洗降低到原信号的10-4倍所需要的时间。
(10) 同位素丰度比测量精度:指某元素的一种同位素与该元素的另一种同位素的丰度比值测定的精密度。
(11) 短期稳定性:在20min 内连续测定同一样品的结果的相对标准偏差。
(12) 长期稳定性:在2h内连续测定同一样品的结果的相对标准偏差。
仪器管理要求与程序
(一) 载气钢瓶的使用规程
(1) 钢瓶必须分类保管,直立固定,远离热源,避免暴晒及强烈震动,氢气室内存放量不得超过两瓶。
(2) 氧气瓶及专用工具严禁与油类接触。
(3) 钢瓶上的氧气表要专用,安装时螺扣要上紧。
(4) 操作时严禁敲打,发现漏气须立即修好。
(5) 用后气瓶的剩余残压不应少于980KPa。
(6) 氢气压力表系反螺纹,安装拆卸时应注意防止损坏螺纹。
(二) 减压阀的使用及注意事项
(1) 在气相色谱分析中,钢瓶供气压力在9.8~14.7MPa。
(2) 减压阀与钢瓶配套使用,不同气体钢瓶所用的减压阀是不同的。 氢气减压阀接头为反向螺纹,安装时需小心。 使用时需缓慢调节手轮,使用后必须旋松调节手轮和关闭钢瓶阀门。
(3) 关闭气源时,先关闭减压阀,后关闭钢瓶阀门,再开启减压阀,排出减压阀内气体,最后松开调节螺杆。
(三) 微量注射器的使用及注意事项
(1) 微量注射器是易碎器械,使用时应多加小心,不用时要洗净放入盒内,不要随便玩弄,来回空抽,否则会严重磨损,损坏气密性,降低准确度。
(2) 微量注射器在使用前后都须用丙酮等溶剂清洗。
(四) 液相色谱的维护与保养
液相系统安装完成后,通常需要进行系统验证测试。 首先保证流通池已经至少冲洗了15min,检测器预热达到30~60min。 之后针对不同的检测器选择不同的测试样品考察仪器的灵敏度、分离度以及峰面积和保留时间的相对标准偏差。
1.溶剂管理系统的维护保养
(1) 缓冲盐流动相要用0.45μm 的水相过滤膜过滤。
(2) 使用过缓冲液时,停泵前要用水清洗泵头,并开启Seal Wash冲洗柱塞杆密封垫1min。
(3) 使用纯水相流动相的管路滤头要放在1:1=有机相∶水的溶剂瓶中,湿灌注后放置。
(4) 抽液后关闭排液阀时,不要太用力拧紧,以不渗液为准。
(5) 更换流动相时,要保证两种溶剂的互溶性,如不互溶,要用一种中间溶剂过渡。
(6) 色谱泵在停用时,应先用水洗去缓冲盐,然后用纯甲醇充满泵头及管路, 并保存在纯甲醇中。
2.液相色谱系统的清洗与钝化 色谱泵吸滤头,进出口阀及管路(包括进样器和检测池)若被污染,应作清洗和钝化处理。 一般采用30% 磷酸水溶液作为清洗剂,用6mol/L硝酸作为钝化剂,先清洗再钝化。 清洗的目的是去除不锈钢管路及系统内的污垢。 钝化的目的是使不锈钢管路的内表面形成光滑均匀的氧化膜。
(1)清洗
清洗液用30% 磷酸水溶液。 30% 磷酸配制:取85% 浓磷酸35ml与65ml水混匀。 清洗步骤如下:
1)取下色谱柱,用两通(union)连接进样器和检测器。
2)用纯水灌注泵头(四元泵的A、B、C、D 四路各为25% )。
3)用30% 磷酸清洗液洗系统(1ml/min流速)45min(四元泵的A、B、C、D 四路各为25% )。
4)换成清水洗至出口水PH显中性。
5) 用纯甲醇过渡,浸润泵头及管路,备用。
(2) 钝化
钝化液用6mol/L硝酸水溶液。6mol/L 硝酸的配制:取浓硝酸40ml 与60ml水混匀。 钝化步骤如下:
1) 在清洗步骤完成后进行钝化处理。
2) 确认清洗用的磷酸已基本洗净。
3) 用纯水灌注泵头(四元泵的A、B、C、D 四路各为25% )。
4) 用6mol/L硝酸水溶液钝化系统(1ml/min流速)45min。
5) 换成清水洗至出口水PH显中性。
6) 用纯甲醇过渡,浸润泵头及管路,备用。
3. 进样器的维护保养 进样针是流路的组成部分,运行中一直由流动相清洗。 进样针外部由软件控制在每次进样前用洗针液清洗。 若注射器内出现气泡,操作Purge Injector功能清除。 样品瓶位置和进样量由软件设定。洗针溶剂根据流动相的不同应有不同(表12-8)。
4. 色谱柱的维护保养
(1) 防止流动相与吸滤头长菌。 每天新配水相流动相。 在关机或系统长时间不用时,请先用水充分清洗系统,然后用适宜的有机溶剂(如乙腈或甲醇)清洗系统。
(2) 确保使用正确合格的过滤膜。
(3) 使用合格玻璃材质的溶剂瓶。
(4) 避免样品不溶微粒与样品沉积。
(5) 使用保护柱延长柱寿命。
5. 检测器的维护保养
(1) 如长时间不用检测器可以关掉光源灯(UV,FL)。
(2) 仅在4h以上不用时,才需关灯,频繁开关灯也会影响灯的寿命。
(3) 不要让缓冲液停滞在检测池内。
(4) 用纯水冲洗,保存在纯甲醇中。
(5) 示差检测器及荧光检测器若与其他检测器串联使用,应将此两种检测器串在其他检测器的后面。
(6) 不用检测器的液晶显示屏时,应将其亮度调暗。
(五)ICP-MS 维护
1. 进样系统维护
(1)取下蠕动泵进样管、雾化室、雾化器及炬管,检查它们是否完好,如有必要应进行清洗或更换。
(2)雾化室及炬管的清洗:石英玻璃制成的部件不可以超声处理。 炬管和雾化室可以在5% 的稀硝酸中浸泡过夜。
(3)雾化器的维护:使用同心型雾化器可能会出现阻塞现象。 阻塞一般由供气或样品中的颗粒物质造成。 遵循以下规则可防止雾化器的阻塞:
1) 在通道中安装低阻抗气体过滤器过滤供气。该法防止气体或气体通道内的颗粒物质沉积在雾化器中。
2) 过滤样品。 建议当样品中的固体物质对分析无关紧要时对样品进行过滤。 由于样品毛细管的设计充分考虑到含固体颗粒的样品的分析,所以分析此类样品时雾化器效率一般不会下降。
3) 如果喷嘴内覆有结晶沉淀,将它浸泡在硝酸稀释溶液中;如果沉淀仍不能去除,使用气体挤压喷嘴冲开阻塞块,也可使用浓度为3% ~ 5%的“王水”冲洗雾化器,最后用去离子水彻底冲洗雾化器。
2. 接口及提取透镜的维护
(1)利用专用工具取下采样锥、截取锥和提取透镜组件。
(2)清洗锥的时候注意不要碰坏锥尖,切勿“硬碰硬”。
1) 用棉棒沾稀硝酸擦洗,尽量不要把锥浸泡在酸中,以延长锥的使用寿命。
2) 由内而外擦洗锥,将棉棒沾稀硝酸擦拭锥体内侧,再擦洗外侧,用棉棒自下而上擦拭,至棉棒上无黑色污染物。
3) 用超纯水充分淋洗锥体,然后用纯净的气体吹干或烘干锥体。
(六) 气质联用仪的使用及注意事项
气质联用仪具有很高的灵敏度,正确而适当的维护对于获得最佳的测定结果,延长仪器使用寿命,减少仪器故障和维修时间是非常重要的。 使用过程中,可参照下表进行日常维护和预防性维护。 具体而言, 应坚持做到以下几点:
(1) 每天检查隔垫(必要时更换),检查进样口衬管,检查色谱柱接头密封性。
(2) 每周检查前级泵油量以及扩散泵油,更换进样口衬管和O形圈。
(3) 每月清洁进样口出口管线捕集阱,检查泄漏(进样口和色谱柱连接部位)。
(4) 每3个月更换气瓶(当气压低于500psi时,1psi=6.895KPa)。
(5) 每6个月更换前级泵泵油,检查校准瓶(必要时重新注满)。
(6) 每年更换扩散泵泵油,重新设置条件,更换内部和外部捕集阱,以及GC上的化学过滤器。
(7) 必要时进行仪器调谐,清洁离子源,更换载气净化管,更换老化部件(灯丝、电子倍增器等),更换色谱柱,润滑密封垫。
(8) 坚持记录电子倍增器和离子源参数的全部调谐数值,用以监控仪器性能,关注高真空和前级泵的真空度。
(9) 气质联用仪的维护计划见表12-9。
表12-9 气质联用仪的维护保养
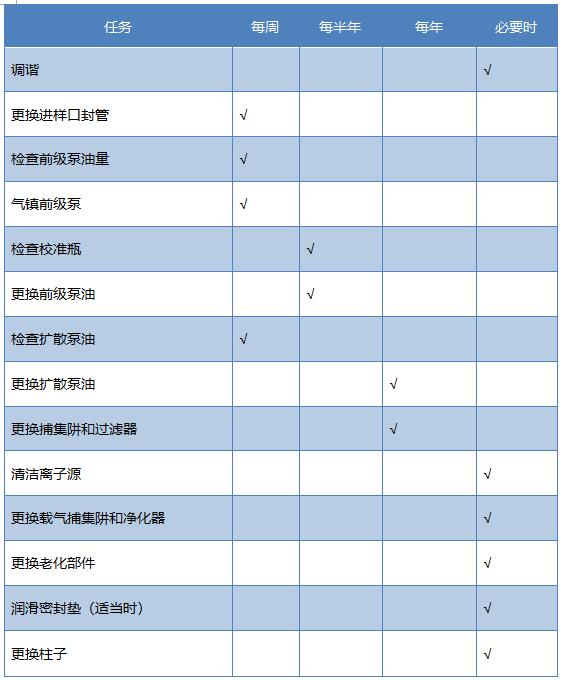
 京公网安备11010102003307号
京公网安备11010102003307号

微信扫一扫
关注医隆网