本栏目由医隆网专家团队审核!
1910 年,Kottman 发明了世界上最早的血凝仪,通过测定血液凝固时的黏度变化来反映血浆凝固的时间。 随后1922 年,Kugelmass 用浊度计通过测定透射光的变化来反映血浆凝固时间。 1950 年,Schnitger 和Gross 发明了基于电流法的血凝仪,这是真正商业化的检测凝血的仪器。 到了20世纪60年代,研发出了机械法血凝仪,70年代以后,由于机械及电子工业的发展,使各种类型的全自动血凝仪先后问世。 80 年代,发色底物法检测原理的出现并应用于血液凝固的检测,使全自动血凝仪除了可以进行一般的筛选试验以外,还可进行凝血、抗凝、纤维蛋白溶解系统等更多项目的检测。 免疫通道的开发又为血栓与止血的检测提供了新的手段,覆盖了大多数的凝血及血栓项目检测,为临床提供了有力的支持。
(1) 半自动血凝仪:目前市售的半自动血凝仪主要由样品、试剂预温槽、加样器、检测系统(光学、磁场)及微机组成。 有的半自动仪器还配备了发光检测通道,使该类仪器同时具备了检测抗凝及纤维蛋白溶解系统活性的功能。 针对半自动血凝仪受人为因素影响多、重复性较差等缺陷,一些半自动血凝仪进行了一系列的设计改进:安装了自动计时装置,以告知预温时间和最佳试剂添加时间;设计了触发式移液器,并将该移液器与仪器进行连接,使得试剂加入的同时启动测试,提高了测试时间的准确性。
(2)全自动血凝仪:该类仪器的基本配置是测试仪主机、计算机系统、输出设备及附件等。对于测试仪主机,一般具有样品吸样/ 加样系统、清洗系统、样品传输系统、测试系统、温度控制系统,而操作显示系统、数据管理系统及数据传输、结果打印、质量控制等功能通常通过计算机系统实现(图4-27)。
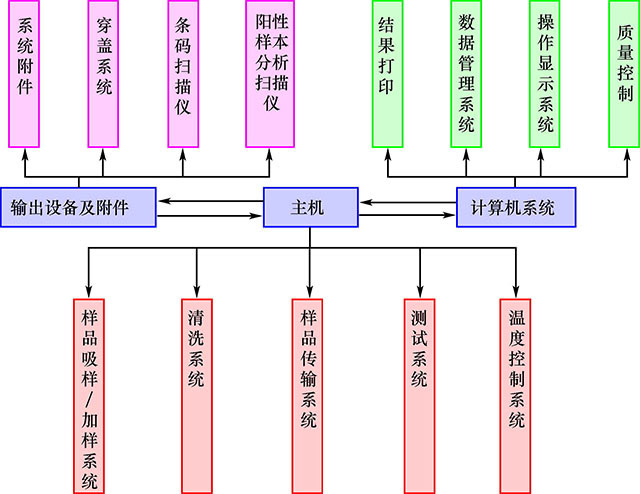
图4-27 全自动血凝仪结构示意
1)样品的吸样/ 加样系统:样品吸样/ 加样系统由加样针及加样针移动单元组成。
加样针针尖和针内外壁工艺要求很高,通过选择和精良的加工,可以避免挂液、滴液,减少残留,降低交叉污染。
有些高端仪器,加样针同时具有预温和液位感应功能。 而预温、液位感应功能的实现尽管给加样针的制作、加工增加了复杂度,但这些功能的实现给临床操作带来了极大便利。
加样针移动单元大多全自动仪器多采用x、y、z三坐标的运动方式。 在结构设计方面多以直线导轨、皮带传动等传动机构。 在机械运动控制方面采取驱动器内置点到点功能、S曲线加速、直线/ 圆弧插补运动、电路细分等技术,并将所有运动加减速、最高运行速度实现参数化调整,是运动定位达到很高的精度。
2)清洗系统:一般包括管路、加样泵及阀门管件。 通过驱动部件和控制电路实现各器件的动作实现流体控制要求。 制造厂商通过调配专用清洗液及洗针液,用以降低不同项目间、不同样品间的交叉污染。
3) 样品传输系统:一般样品存放装置可以放置几十份样品。 吸样针将被测标本吸取后放于标本预温盘的测试杯中,可供重复测试,自动再稀释和连锁测试之用。
一般血浆样品由传送装置依次向吸样针位置移动,也有通过吸样针的移动及液位感应功能将固定位置的样品进行吸取,并移动到测试杯位置进行加样。 多数仪器还设置了急诊位置,可以使常规标本检测必要时暂停以服从于急诊标本的优先测定。
4)温度控制系统:为避免试剂的变质,全自动血凝仪通常设计了试剂冷藏位,各厂家的冷藏位从4~16℃不等,至少可放置常用测试项目的试剂,有些可同时放置达70多种试剂。
需要加热的部分有样品预温区、测试区、试剂区一部分,一些较为复杂的加样针也具有快速加热功能。
通常的加热温度控制在37℃,温漂及温度梯度不宜过大,用以减少因孵育造成的检测误差。
5) 测试系统:检测血浆的凝固可以通过凝固反应检测法检测,即当纤维蛋白凝块形成时,检测散射光吸光度的变化;或通过凝固点检测法检测,即计算达到预先设定好的吸光度值时的凝固时间;而磁珠法则是通过测定在一定磁场强度下小钢珠的振动幅度变化来测定血浆凝固点。 发色底物法及免疫法是检测反应液的吸光度变化来反映被检测物质的活性或含量。
6) 计算机系统:目前的全自动血凝仪多数配备了计算机(计算机主机、显示器和打印机)。 上位机程序大多可实现操作显示系统、数据管理系统及数据传输、结果打印、质量控制等功能。 根据设定的工作程序,并配合测试仪主机的控制系统,共同指挥血凝仪进行工作。 同时上位机程序编制了人性化的数据管理系统,将检测系统得到的测量数据进行分析处理,最终得到测试结果。 并将患者的检测结果进行储存,记忆操作过程中的各种失误及进行质量控制有关的工作。
计算机与全自动血凝仪主机的控制及通讯方式见图4-28。
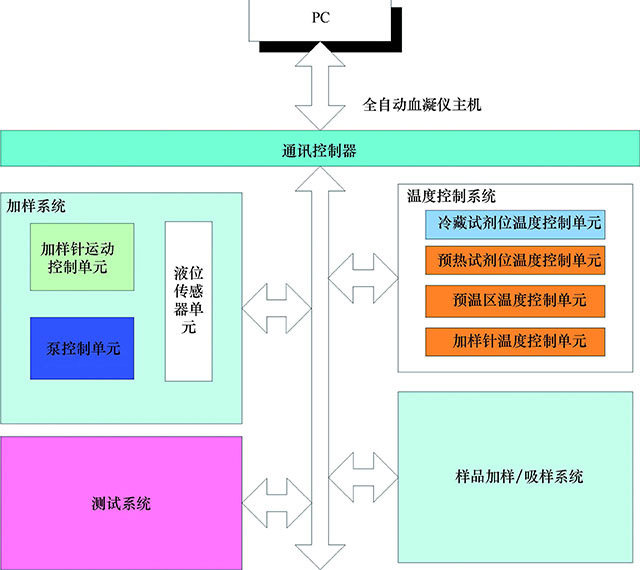
图4-28 主机控制及通讯方式示意
此外,计算机系统通常还考虑设计了各类报警系统、功能参数化/ 模块系统、运动控制测试系统、专用调试系统。
7) 附件。
8) 主要有系统附件、穿盖系统、条码扫描仪等。
1. 全自动凝血因子分析仪行业标准 目前国内已经有全自动凝血因子分析仪的行业标准(YY/T 0659-2008),在标准中规定了全自动凝血因子分析仪的术语和定义、分类和组成、要求、试验方法、标志、标签、使用说明、包装储运输和储存。标准中规定了仪器用于检测血浆凝血酶原时间(PT)、活化部分凝血活酶时间( APTT)、纤维蛋白原(FIB)、凝血酶时间(TT)检测的技术要求。其中有以下一些内容:
2. 血浆凝固实验血液标本的采集及处理指南 国内已经将美国临床及实验室标准研究院(Clinical and Laboratory Standard Institute ,CLSI) 的专业指南《血浆凝固实验和分子凝血检测的血液标本的采集、运输和处理指南》( Collection,Transport,and Processing of Blood Specimens for Testing Plasma-Based Coagulation and Processing of Blood Specimens for Testing Plasma-Based Coagulation Assays and Molecular Hemostasis Assays; Approved Guideline-Fifth Edition ) (H21-A5)中的部分内容转化为国内的行业标准《血浆凝固实验血液标本的采集及处理指南》(WS/T359-2011)。该指南规定了血浆凝固实验血液标本的采集及处理的要求。
目前的全自动凝血因子分析仪可以进行凝血、抗凝和纤维蛋白溶解系统功能的测定。
(1)凝血系统:可以进行凝血系统的筛选实验,如凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、凝血酶时间(TT)测定,也能进行单个凝血因子含量或活性的测定,如纤维蛋白原、凝血因子Ⅱ、Ⅴ、Ⅶ、Ⅹ、Ⅷ、Ⅸ、Ⅺ、Ⅻ等。
(2)抗凝系统:可进行抗凝血酶(AT)、蛋白C(PC)、蛋白S(PS)、抗活化蛋白C(APCR)、狼疮抗凝物质(LAC)等测定。
(3)纤维蛋白溶解系统: 可测定纤溶酶原(PLG)、α2-抗纤溶酶( α2-AP )、D-二聚体( D-Dimer)等。
(4)临床用药的监测:当临床应用普通肝素(UFH)、低分子量肝素(LMWH)及口服抗凝剂如华法林时,可用凝血因子分析仪进行监测以保用药安全。
1.分析前的质量控制
(1) 抗凝剂选择及用量
1) 抗凝剂选用105 ~ 109mmol/L、3.13% ~3.2(通常描述为3.2% )枸橼酸钠(Na3C6H5O7·2H2O),其他抗凝剂,如肝素、EDTA、草酸盐等均不得使用。 当抗凝剂与血液混合后的终浓度通常10.9~12.9mmol/L。
2) 抗凝剂与抽血量的比例为1:9。
3) 若患者血细胞比容(PCV)大于55% 或小于20% 时,通常需要调整抗凝剂的用量。 抗凝剂的用量可按下列公式进行调整:
X=需用的抗凝血量×[(100-PCV) / (595-PCV)]
其中:X为需用的抗凝剂的量,单位ml;PCV 为血细胞比容,单位为% 。 例如:需要5ml 抗凝血,患者的PCV=20% ,则需要的抗凝剂X=0.7ml。
(2) 标本的采集
1) 时间:清晨空腹,确认患者服药情况。
2) 部位:一般取前肘静脉血。
采血时应一针见血,切忌反复穿刺,避免溶血、血小板因受刺激而发生聚集(如发现溶血应重新抽血)、将组织液抽到注射器中或将气泡混入。 血液与抗凝剂混匀时,手法应轻柔,不可剧烈晃动,以免产生气泡影响加样针的液位感应功能。
(3) 采用质量合格的标准真空采血管
1) 采集量:采血量不少于2ml,过多或过少都可能对测试过程和结果产生影响。
2) 颠倒混匀,避免用力振荡破坏凝血蛋白。
(4) 样品的制备:将混匀的抗凝血在25~32℃ 下离心,转速是2000~2500r/min,时间控制在10min 左右,待离心机自然停止后取出( 如出现溶血现象应重新采血),试管内上清液体即为贫血小板血浆(PPP)。 分离血浆时,应使用塑料吸头和容器。
(5) 样品的放置
1) 凝血测试在18~24℃ 下,PT测试样品应在24h 内测试;APTT测试样品应4h内测试;其他测试(如FIB、PC、因子V、因子Ⅷ等)应4h 内测试。
2) 凝血测试如果不能立即进行,样品可在4℃下保存2h。 如果PT测试样品不能在24h内或APTT及其他测试不能在4h内测试,血浆样品应放置在-20℃以下冰冻保存2周,-70℃保存6 个月。冰冻样品应在37℃下迅速解冻,并立即测试。 冰冻过的样品,可能会影响APTT测试。
3) 建立不合格标本的拒收和拒检制度,检验前应对标本量、凝块、溶血、黄疸、压积等进行目测过筛。
2. 分析中的质量控制
(1) 仪器
1) 检测的环境温度:15~30℃。
2) 仪器各温控器件是否达到稳定的温度控制范围,如样品预温区、测试区、试剂储存区、试剂加样臂/ 针。
3) 确认仪器已经过校准并处于有效校准状态。
4) 确认检测项目需设定的参数均符合反应体系所需要求。
5) 确认设备定期进行了保养与维护,并处于良好的使用状态。
6) 全自动设备已添加好测试耗材,如正确的测试杯、清洗液等。
(2) 试剂
1) 选择与仪器匹配、质量可靠、性能稳定的试剂。
2) 试剂稳定性的确认:试剂在仪器内的稳定性不应该超出厂商对稳定性的声明。 准备足够的试剂以保证整个检测过程的需要。 试剂的准备可能包括重组、搅拌、平衡到一定的文档等。 至少检测2个浓度水平的新鲜质控血浆,每个浓度3份。 计算均值,建立基线值,它代表了在0 时刻的值。 根据其他研究建立0时刻的均值可接受范围(±10% ,±2s,±一个绝对值),并确认其重复性在方法的总精密度范围内。 在0时刻后的周期时间间隔内,按照厂商的要求进行检测,以确认仪器方法稳定性声明。 每个时间点计算各均值,试剂都可被认为是稳定的,直到两个值在连续超出0时刻建立的范围。
3) 在试剂使用前,务必详细阅读试剂盒内的说明,并严格按其说明书的规定使用及保存。
4) 确认试剂在有效期内。
5) 冰冻试剂不能反复冻融。
6) 不同批号、不同厂家、不同成分、新旧试剂不能混合使用。
7) 严格使用试剂说明书规定复溶液进行冻干试剂复溶。 如果使用蒸馏水复溶,应严格保证蒸馏水质量。 试剂复溶时,应避免剧烈摇晃,以免产生气泡对测试结果造成影响。
8) 使用不同批号和厂家的凝血试剂都需要重新做校准,校准所使用的校准品应为具有溯源性的校准血浆。
(3) 设备使用:检测过程中严格按仪器厂家提供的产品使用说明书,以及SOP文件进行设备操作。 并及时处理设备报警,避免试剂、标本长时间加载而导致的测试结果偏差。在仪器使用前应该制定一个标准操作规程,使工作人员的操作适当。 每个程序应包括所需的试剂、试剂的配制、仪器的操作、进一步稀释的解释和干扰物质的问题。
(4) 室内质量控制
1) 质控品的选择:选择与试剂匹配的质控品。至少选择2个水平质控品,其中一个质控品应在正常参考范围内,另一个应超过正常参考值1.5倍以上。 如果有条件的可选择1个正常质控品,2个异常质控品。
2) 建立质量控制范围:建立一个暂时的目标范围至少需要对2种不同浓度水平的9份血浆质控物进行检测,至少持续3天。 计算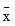 ±3s 作为暂时的质控范围。
±3s 作为暂时的质控范围。
以特定的时间间隔继续检测两水平的质控血浆。 达到厂商或机构要求的质控数量后,所得的数据计算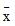 ±3s 即可用于日常性能监测。
±3s 即可用于日常性能监测。
3) 校正曲线:检测项目应该有一个校正曲线以校正报告单元的形式报告。 用于建立曲线的血浆应该溯源到标准血浆,如WHO 和NISBC 标准。 对于不能溯源到国际标准品或校准程序的项目,应能溯源到厂商校准品。 每个校正曲线都应该有多个(至少3个)稀释度的血浆通过与处理标本相似的方法检测所得。
校正曲线的稳定时间被认为和质控物质在建立的范围内一样长。 有必要根据仪器进行周期性校正。 改变试剂、仪器或者失控则要重新校正。
4) 质控频次与方法:每天在标本检测前,应进行正常及异常值质控血浆、正常对照血浆的检测。非手工法凝血试验,每8h必须做2个水平质控一次或每次更换试剂后进行一次。 手工法凝血试验,测试患者标本前,必须做2 个水平质控一次或每次更换试剂后一次,患者和质控必须双份测定。 每批试验必须有正常对照。 发现问题后,查找原因及处理,保证结果准确、可靠。
正常对照血浆的制备:至少20 份健康人血浆,年龄在10~55岁的男女个体。 排除服药者,在平静、空腹状态下抽血,分离血浆后混合在一起,并分装至小容器内,-80℃冻存或冷冻干燥后使用。
5)质控结果的确认与失控处理:每次得出质控结果后,都应记录在质控图内。 如发现质控图超过原标定的平均数2s 时,应逐一检测仪器、试剂和质控血浆有无问题,并加以校正。 否则不能发出报告。
操作人员在进行质量控制时,如发现了质控数据违背了控制规则,应记录失控结果,违背的质控规则。 当得到失控信号时,可以采用如下步骤去寻找原因:
1) 立即重测定同一质控品,此步主要是查明人为误差,每一步都认真仔细地操作,以查明失控的原因。 另外,这一步还可以查出偶然误差,如是偶然误差,则重测的结果应在允许范围内。
2) 重新开一瓶质控品,重测失控项目。 如果重新开的质控血浆结果正常,那么原来那瓶质控血清可能过期或在室温放置时间过长而变质或者被污染。
3) 新开一批质控品重做失控项目,如果结果在控,说明前一批血清可能都有问题,检查它们的有效期和储存环境以查明问题的所在。
4) 更换试剂重新测定,如结果在控,则为试剂问题。
5) 仪器的维护后重测,如结果在控,则为仪器原因。
6) 对仪器进行重新校准,重测质控项目,看是否在控。
(5) 操作人员的培训:所有的操作人员都必须培训,熟练掌握仪器工作原理、操作规程、保养维修及常见故障排除。 严格按仪器操作规程,禁止简化任何程序。 认真执行试剂盒说明书的操作,注意试剂的有效期查验,防止错用混用。 厂商应该对实验负责人进行强化培训。 负责人再对其实验室的其他人员进行培训。 负责人应该给新仪器的操作者解释试剂的配制、仪器的操作限制及干扰物质。
3. 分析后的质量控制
(1) 报告运送及临床反馈
1) 测试结束后,实验室负责人应授权其他人员对检测结果进行审核,并由实验室负责人签发测试报告。
2) 对于异常结果应进行复检,并与原检测结果进行比较,如无明显差异,可申请结果审核,并出具报告。 如与首检结果差异较大,应先查明原因。 如已排除实验室及测试原因,应联系临床科室进行原因分析。
3) 对于标本不符合检测条件的,应在报告中有明显标注。
4) 实验室应该告诉所有的用户(临床医生、护士和药师)关于参考范围和质量范围,以及它们的改变。 否则,患者的诊治会受到影响。 在告知前不能使用新的参考范围。
5) 实验室必须和药师沟通改变所有用于肝素治疗的公式,而且这些改变应该及时告知临床医生和护士。 输血的临界值基于PT/ INR 和APTT,实验室必须与临床医生及输血科沟通,改变输血指征。留存被检标本,备复检或复查使用。
6) 仪器必须以清新可见的方式记录所有相关的数据和图表。 包括所检验时间、操作人员、使用的试剂批号,还必须能保持所使用的校正曲线,用于多种方法分析同一物质的对比。
7) 每个项目的质控程序应该以简易的方式保存,定期的质控数据应该处理后以简明的方式展示,长期的质控数据应该保存。
(2) 室内质控的数据管理:室内质量控制可监测和评价检测系统的精密度和稳定性,也可间接评价检测结果的准确性。 室内质控的目的是监测测定过程,当出现医学上重要的误差时,用适当的质控方法警告分析人员。 一般来说,实验室通过测定质控品来检查检验结果的质量,并将质控结果画在质控图上,观察质控结果是否超过质控限来决定是否失控。 实验室最常用的是Levey-Jennings 质控图。 一些全自动设备还运用Westgard多规则质控方法,来判断检验结果的质量,是否需要做系统的纠正,患者检验结果是否可接受。
在实际工作中,只有当根据质控图判断分析批在控时,方能报告患者标本的测定结果。 当判断分析批为失控时,则测定过程有可能存在问题,此时重要的是要查清是真问题还是假失控。 如是真问题,则应在解决问题后重新测定。 如是假失控,可由实验室负责人作出重审决定,发出检验报告。 每分析批至少测定2个质控品。
每个实验室应每月或定期对室内质控数据进行统计处理,应对当月或该统计期的所有质控数据进行汇总和统计处理,计算的内容应包括:
1) 每个测定项目原始质控数据的平均数、标准差和变异系数。
2) 每个测定项目除去失控数据后的平均数、标准差和变异系数。
每个测定项目所有质控数据的累积平均数、标准差和变异系数。
3)保存室内质控数据。 保持当月或统计期所有项目的原始质控数据;所有项目质控数据的质控图;平均数、标准差、变异系数及累积的平均数、标准差、变异系数;以及当月的失控报告单。
对室内质控数据进行周期评价。 定期要对当月或本统计期室内质控数据的平均数、标准差、变异系数及累积平均数、标准差、变异系数进行评价,查看与所得各月或其他统计期的平均数之间、标准差之间、变异系数之间是否有明显的不同。
1)室间评价:实验室必须积极参加有临检中心组织的室间质评活动,了解本单位PT测定的准确性。 回报时附仪器型号和试剂品牌及批号信息,以供比较。
2)患者投诉处理:质量和服务是检验工作的核心,检验人员要正确对待来自临床和患者的投诉,根据来自不同方面的意见,不断地改进和增强质量和服务意识,检验科室主任是第一责任人,负责接待、处理投诉。 每位职工都必须认真接受患者和临床医师在服务和质量上的投诉,不得推诿。 科室实行“首问、首接负责制”,对任何投诉均必须受理。
接受患者投诉的处理程序是:接待记录→查明原因→耐心解释→有错赔礼→是错必纠→必要时赔偿患者的经济损失→让投诉者满意。
接受临床医师投诉的处理程序是:接待记录→查明原因→及时改正→改进工作→避免同类错误。
科室要根据实际情况召开科会对投诉记录进行归纳和分析,找出问题所在,提出改进方案,为进一步做好质量和服务工作打下良好基础。
1.人员的要求 工作人员上岗前必须作好培训,熟练掌握仪器工作原理、操作规程、保养维护及常见故障排除。
2.合适的环境 足够和适宜的空间,按厂家要求提供合适的温度、湿度。
3.仪器的验证 应用流程质量保证维护建立完善的仪器验证应用流程。
(1)批内精密度的验证:将正常混合血清重复测定20次,观察其批内精密度。
(2)批间精密度验证:使用髙低值校正血浆,测定PT、APTT、TT、纤维蛋白原(FIB),每天1次,共20天。
(3)准确性试验:使用正常及异常值校正血浆,测PT、APTT、TT、FIB,将结果与靶值比较,观察偏差是否在允许范围内。
(4)相关性试验:用该全自动分析仪和手工法检测20份血浆的PT、APTT、TT、FIB,并将其结果进行比较。
(5)干扰试验采用标准干扰物(溶血性血红蛋白、结合胆红素、非结合胆红素和乳脂蛋白)分别加入到试验血浆中,再测定各种浓度干扰物2试验血浆的PT、APTT、TT和FIB。
4.试剂的质量保证
(1)用商品试剂盒时,对于国家规定应有生产许可证、注册登记证的品种,决不能使用没有生产许可证、注册登记证的商品试剂盒,尚未规定应有生产许可证、注册登记证的品种,生产厂家应提供该产品的性能规格以及质量保证书。
(2)实验室应根据仪器制造商说明的要求来选择和使用校准品及质控品。实验室自行选用的校准品或质控品,应有实验依据证明其不影响检验结果和报告的准确性和可靠性。
(3)试剂的贮存:血凝试剂盒均为生物制品,容易受环境因素影响而降低甚至失去活性,因此,运输、贮存应严格限制在2〜8℃,使用过的试剂一般存放冰箱(2〜8℃),不得超过3天。
(4)试剂的应用:按照试剂的使用说明,严格操作准确溶解试剂,复溶后的PT及CaCl2溶液必须放置预温至37℃备用。
(5)当试剂、溶液、培养基、校准品、质控品和其他供应品超过其有效期,已经变质或者质量不合格时,不能使用。只有当生产厂家或权威机构出具书面证明或者实验室有充足依据证明其不影响检验结果和报告的准确性和可靠性时,方可在规定的延长期间使用。试验所用的标本质量、试剂、质控液、蒸溜水、吸管、冰箱以及它们分别的处理方式,都是止血凝血试验结果质量正确与否的关键。溶解试剂时,在部分试剂不能一次性用完时,比如质控液采用分装贮存-20℃的办法,按照国际标准化组织颁布的ISO15189文件的要求,所有影响实验结果的要素和环节都应协调和统一。
5.定标每日检测标本前应用仪器配套的定标物对仪器进行定标。
6.参考范围 PT、APTT、TT、FIB、纤溶酶原(PLG)是判断机体止血与凝血系统病理变化的重要指标,也是临床溶栓、抗凝治疗及手术前的必要检查项目。因仪器、试剂不同,会得出不同结果,故很难统一规定参考值。各实验室可根据自己的检测系统制定本实验室的参考值。
7.作好室内质控是仪器是否处于最佳工作状态并确保检验结果准确性的重要保证。
(1)质控品(校准品)必须按患者标本那样进行检验。
(2)使用质控品时,实验室要重复检测来决定每一批号质控品在本室的统计学参数(如均值、标准差、变异系数等)。定值质控血清的值,可用来作为室内质控的靶值,但要保证声称的定值和所用的方法学和仪器相匹配,并被实验室所证实。进行室内质控时,可以对定值质控血清的靶值进行修正。质控品不宜反复冻融,取出后37℃速融,20分钟后上机进行质控检测,才能确保室内质量控制的稳定性。
(3)在报告检验结果前,质控品结果必须达到实验室设定的接受标准。
(4)纠正措施:实验室必须建立纠正措施,以维护实验室有准确和可靠的检验结果。下列情况时,实验室必须将纠正措施记录并写成文件。
1)质控和校准的结果未达到实验室确立的标准,此时应对不能接受的那次操作的所有检验结果进行评估,以决定检验报告是否受到不利影响。实验室必须采取纠正措施以保证检验结果和报告的可靠性。
2)如发出的检验结果有错误,实验室必须立即通知申请者或者使用此错误报告的人员;立即对申请者或者使用此错误报告的人员发出纠正的报告;保存原来以及纠正报告的副本1年。
3)质控记录:实验室必须按本要求中所规定要求记录的项目进行记录,并形成文件。
8.室间质评每年参加卫生部和WHO室间质控。
 京公网安备11010102003307号
京公网安备11010102003307号

微信扫一扫
关注医隆网