本栏目由医隆网专家团队审核!
免疫层析技术出现于20世纪80年代初期,是将免疫标记技术与层析技术相结合的一种新型检测技术。1962 年,Feldherr 和Marshall 首次报道可将胶体金颗粒作为电子显微镜下的示踪标志;1971年,Faulk和Taylor发明了胶体金标记蛋白质的方法,应用于免疫组化;1973年,Frens G发明了柠檬酸钠还原氯金酸制备胶体金的方法;1984年,第一次利用胶体金在硝酸纤维素膜上实现了抗原的可视化检测。
免疫层析的核心技术是以条状纤维层析材料为固相,通过毛细管作用使样品溶液在层析材料上泳动,并同时使样品中经标记物标记的待测物与包被在层析材料上针对待测物的抗原/抗体发生高特异、高亲和性的免疫反应,富集在检测线上,通过标记物的颜色或光电磁等信号放大效应达到检测目的。常规的试纸条结构见图1。
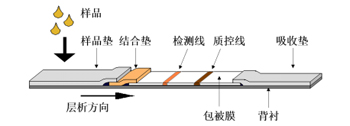
图1 免疫层析试纸条结构
免疫层析技术根据标记物种类的不同,可以分为胶体金免疫层析技术(colloidal gold immunochromatography assay,GICA)、荧光免疫层析技术(fluorescence immunochromatography assay,FICA) 、量子点免疫层析技术(quantum dot immunochromatography assay,QDICA) 等,其原理大致相同,一般分为夹心法和竞争法,而夹心法又分为双抗原夹心法和双抗体夹心法。在此就胶体金免疫层析技术对免疫层析技术原理加以详细介绍。
1、夹心法
夹心法即待测物中的抗原或抗体,与检测条带处的抗体或抗原,以及胶体金标记的抗体或抗原发生特异性的结合,形成三明治型的复合物。检测信号与待测物质的浓度成正比。夹心法常用于检测含有两个或两个以上抗原决定簇的大分子物质。检测原理如图2-2 所示。将免疫试纸条置于平整的台面上,加入待测物质,如待测样本中含有相应的物质,则该物质可与金标抗体和检测线抗体结合成一个双抗体夹心免疫复合物大分子,多余的金标抗体继续层析,在质控带(C)处,与质控带处金标抗体二抗结合,随着金标抗体的累积,质控区呈现红色。因此阳性结果为检测区(T)和质控区(C)都出现红色条带,阴性结果为仅质控区(C)出现一条红色条带,如质控区(C)未出现红色条带,则认为试纸条失效。
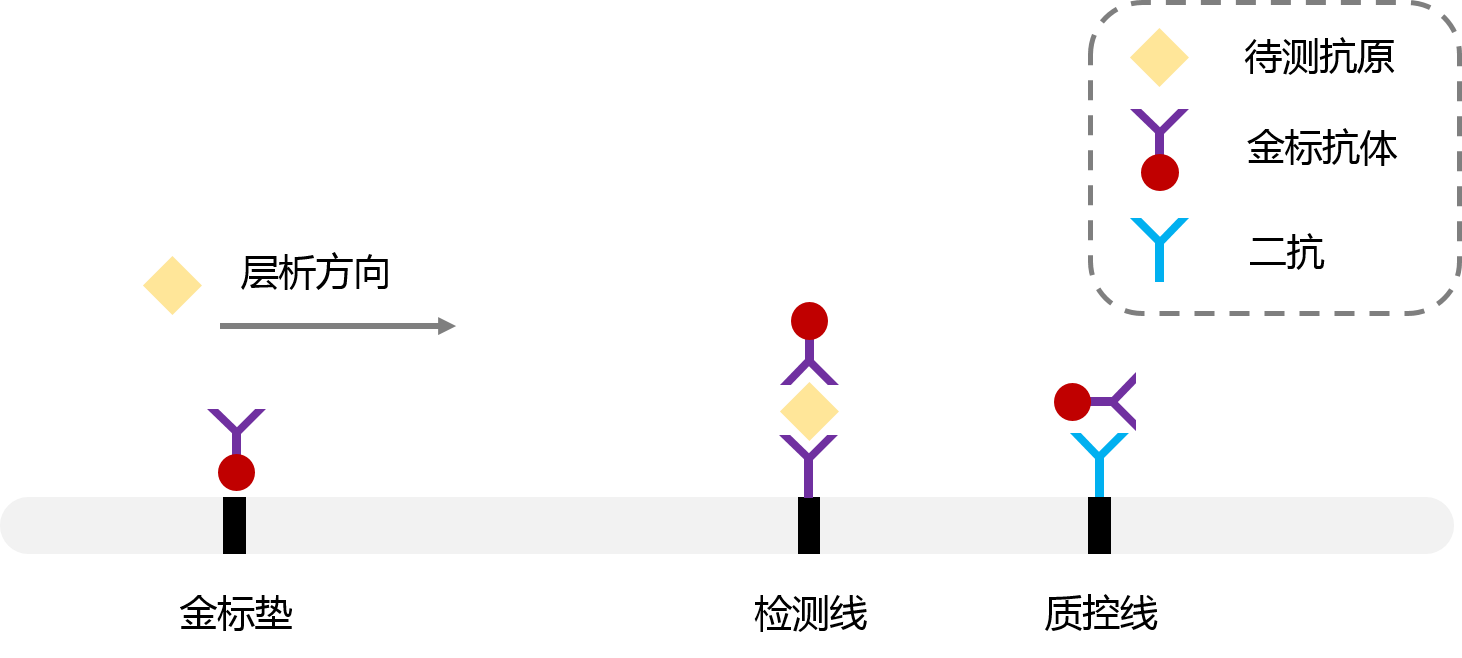
图2 双抗体夹心法原理图
2、竞争法
竞争法即待测物中的抗原和检测条带处的相同抗原竞争结合胶体金标记的抗体,检测信号与待测物质浓度成反比。一般用于检测小分子的抗原决定簇和半抗原重组物质。检测原理如图3所示。将免疫试纸条置于平整的台面上,加入待测物质,待测物质中的抗原或抗体与检测线上的抗原或抗体,竞争性结合胶体金标记的抗体。当待测物中含有相应的抗原或抗体时,检测带变浅或无色,当待测样本中不含相应的抗原或抗体时,检测带显色。多余的抗体继续层析,当其层析至质控带时,由于不存在竞争结合的关系,所以质控区的抗体不断累积,进而显色。因此阳性结果为仅质控区(C)出现一条红色条带,阴性结果为检测区(T)和质控区(C)都出现条带,如质控区(C)未出现红色条带,则认为试纸条失效。
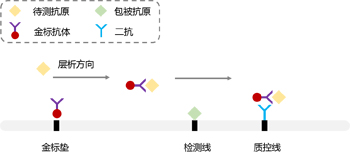
图3 竞争法原理图
1、国际上已有的相关准则和标准
在美国,POCT 是由认证/授权机构、POCT 委员会、POCT协调员共同组织管理的,同时由FDA 监管。它的认证/授权机构是卫生保健组织鉴定委托委员会(JCAHO)对POCT认可;并与医疗保险和医疗补助服务中心(CMS)提出、制订POCT 的政策、各种规定程序及其格式。美国病理学家学会(CAP)也认可POCT,并参与规章的定义和鉴定指导方针的制定。因此JCAHO、CMS、CAP 是POCT 的认证/授权机构。又据文献介绍,美国CLSI规定:①开展POCT的主要目的是方便患者,快速而又价廉地得到可靠的检验结果;②POCT可允许非检验人员操作,但任何地方开设POCT都必须接受政府有关部门的审批,有相应的规章制度、人员培训资格证书、使用仪器的准入、规范的检验程序;③必须参加政府指定的室间调查评价,随时接受政府有关部门的质量评估,不合格者将被取消资格;④在医院内的POCT和医院外的要求不一样,医院内开展POCT必须按照国家、地方及医院有关临床检验及特定的要求进行,使用POCT方法须和医院检验科的检测方法进行方法学比对,被认可后方可使用;⑤每个POCT项目都必须有书面操作手册,含试剂、仪器、校正、质量控制、操作步骤、结果报告程序、方法局限性、参考范围、注意事项等。
2、在我国相关规定
为了保证医院内POCT稳步有序发展,国家质量监督检验检疫总局和国家标准化管理委员会针对POCT的应用范围,于2013年10月联合发布“Point of care testing(POCT)国家标准”(ISO/22870:2006,IDT),“ 即时检测—质量和能力的要求”(requirements for quality and competence)。该标准规定了适用于即时检测(POCT)的专用要求,并与GB/T22576—2008结合使用。该标准的要求适用于在医院、诊所或提供流动性医疗服务的医疗机构所进行的即时检测。该文件于2014 年2月实施。
3、行业内管理相关部门
委托医学会检验分会成立POCT专业委员会起草管理文件,有些地区和医院已经自行制订管理制度并开始实施,大致包括以下内容。
(1)成立管理机构:POCT 质量管理小组由分管院长、医务科、质管科、检验科、ICU、各应用科室的相关人员组成。
(2)仪器、试剂条的准入与注册。
(3)进行POCT 操作人员培训及考核。
(4)指导、敦促有POCT 的各临床科室,制订可行性操作文件,纳入制度化管理。
(5)坚持进行室内质量控制,落实质控措施,定期做好室间质评调查和与临床实验室的比对工作。
附录1:即时检测 质量和能力的要求Point-of-care testing(POCT)—Requirements for quality and competence (ISO 22870:2006,MOD)
 京公网安备11010102003307号
京公网安备11010102003307号

微信扫一扫
关注医隆网